Как узнать паркинсона болезнь
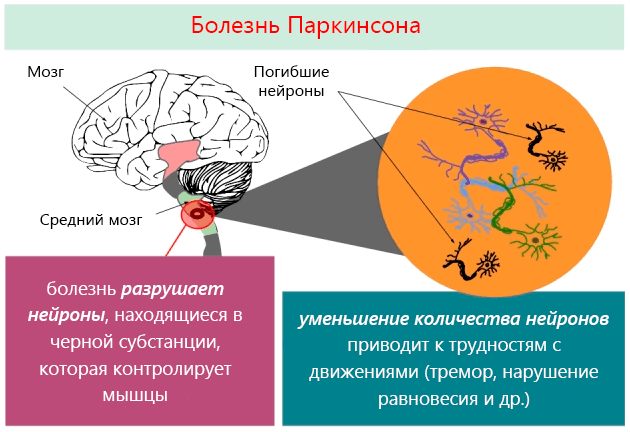
Болезнь Паркинсона – заболевание головного мозга, при котором происходит нарушение движений человека. Развивается из-за снижения количества нервных клеток, которые вырабатывают специальное вещество – дофамин. Проявления болезни Паркинсона: нарушения походки, дрожание рук и ног.
Причины нехватки дофамина в головном мозге до конца не изучены. Выделяют множество факторов: наследственность, вредное воздействие окружающей среды, старение.
Чаще симптомы болезни Паркинсона выявляются у людей пожилого возраста. Характерные нарушения постепенно усиливаются, приводя к инвалидности. В настоящее время не существует методов лечения, приводящих к полному выздоровлению, так что терапия направлена на облегчение состояния больного.
Первичный паркинсонизм, дрожательный паралич.
Parkinson’s Disease, Parkinsonism.
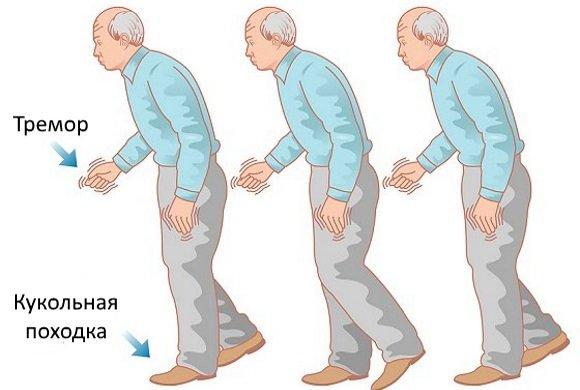
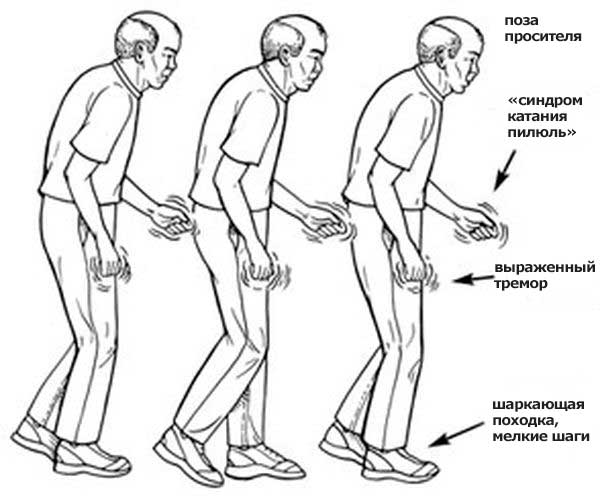
Первые проявления болезни Паркинсона незначительны: подавленность без очевидных причин, монотонность речи, замедленность движений, ходьба мелкими шагами, дрожание рук, снижение количества движений типа морганий, размахивания руками при ходьбе.
Со временем симптомы болезни становятся более выраженными.
Общая информация о заболевании
Заболевание известно достаточно давно – впервые его описал английский врач Джеймс Паркинсон в 1817 году. Болезнь Паркинсона в 1,5 раза чаще встречается у мужчин, чем у женщин. Проявления заболевания развиваются при гибели значительной части нервных клеток, производящих специальное химическое вещество – дофамин. Это вещество влияет на взаимосвязь между структурами головного мозга, которые обеспечивают согласованную работу мышц, необходимую для нормальных движений человека. Существует множество мнений относительно причин гибели этих клеток:
Другое название болезни Паркинсона – первичный или идиопатический паркинсонизм. Идиопатический означает, что причина болезни не может быть выявлена. Так же выделяют атеросклеротический паркинсонизм, паркинсонизм, вызванный лекарственными препаратами и другие, то есть виды паркинсонизма, когда есть причина, вызвавшая проявления паркинсонизма.
Кроме того, существует много заболеваний, симптомы которых схожи с болезнью Паркинсона (например болезнь Вильсона).
Кто в группе риска?
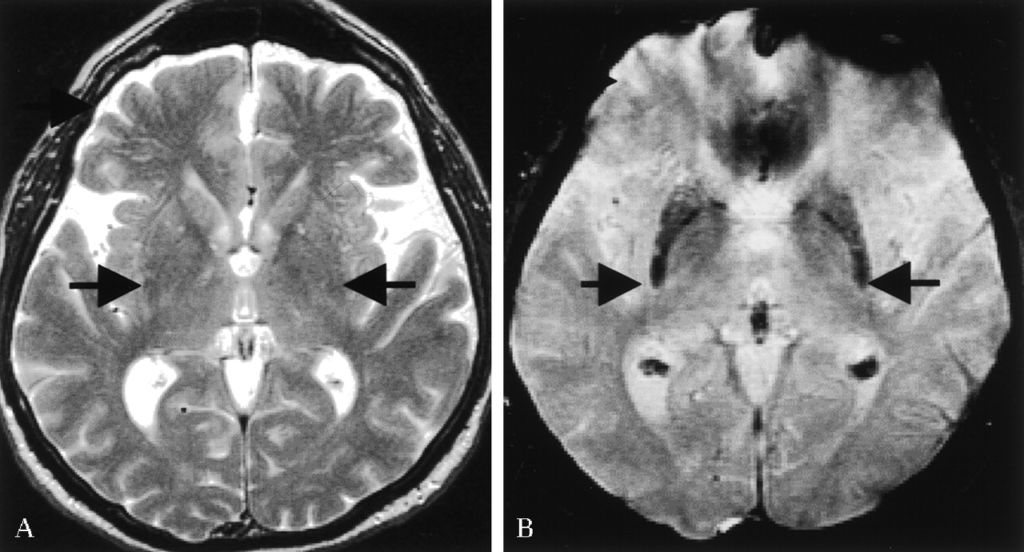
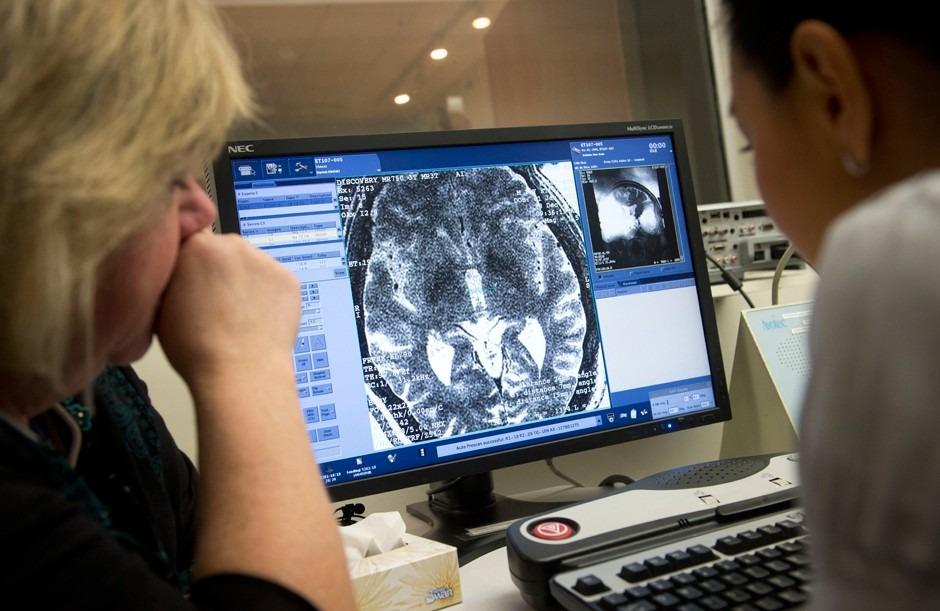
Диагностикаболезни Паркинсона основана на наличии характерных симптомов болезни. Специальных исследований, подтверждающих болезнь Паркинсона, нет. Комплексное обследование пациента включает в себя магнитно-резонансную томографию головного мозга (МРТ), которая позволяет исключить опухоли, очаги нарушения кровообращения в головном мозге. При болезни Паркинсона изменения головного мозга на магнитно-резонансных томограммах, как правило, отсутствуют.
Пациентам с нетипичными проявлениями болезни могут назначаться дополнительные исследования на наличие других заболеваний, имеющих схожие проявления с болезнью Паркинсона.
Обездвиженность, нарушение мочеиспускания, тяжелое состояние больных способствуют развитию воспалительных процессов в организме. В целях выявления данной патологии проводят общий анализ крови, анализ мочи.
Объем проводимого обследования зависит от конкретной клинической ситуации и определяется лечащим врачом.
Лечение болезни Паркинсона направлено на облегчение состояния больного. Методов, позволяющих полностью преодолеть болезнь, не существует. Используются препараты, замещающие недостаток дофамина в головном мозге. Большую роль играют специальные упражнения, позволяющие укреплять определенные мышцы. Это не останавливает развитие болезни, но способствует облегчению состояния больных, улучшению речи, жевания, глотания, способности ходить. В случаях неэффективности терапии проводится хирургическое лечение, направленное на глубинные отделы головного мозга, контролирующие движения.
Профилактики болезни Паркинсона нет, хотя в настоящее время ученые ищут методы излечения от нее и способы восстановления утраченных двигательных функций.
Болезнь Паркинсона: причины, признаки и симптомы, стадии, лечение
Что такое болезнь Паркинсона (БП)? Это хроническая патология ЦНС с постепенно прогрессирующим течением, в основе развития которой лежит дегенерация и гибель в черном веществе головного мозга нейронов, синтезирующих дофамин. Дофамин известен как нейромедиатор, который у здорового человека в достаточном количестве поставляется аксонным транспортом к подкорковым ядрам мозга. Этот процесс позволяет держать под контролем двигательную активность и тонус мышц. При болезни Паркинсона выработка биологического вещества сокращается из-за нейродегенерации (разрушения) дофаминовых нейронов, которые постепенно гибнут.
По мере темпов отмирания нервных клеток, синтез дофамина все больше и больше угнетается. Когда уровень погибших нейронов достигает критической отметки, заболевание начинает проявляться. У человека развиваются серьезные двигательные расстройства, которые становятся тяжелейшим испытанием для больного и его родных. Ввиду хронической дегенерации структур черной субстанции головного мозга патологический процесс носит необратимый и постоянный характер.
Причины развития Паркинсона
По сути, в головном мозге каждого человека в некоторой мере нейроны обречены на погибель, что является вполне естественным для физиологии процессом. Специалистами рассчитана даже закономерность утраты нервных клеток мозга у абсолютно всех людей: за 10 лет жизни безвозвратно погибает примерно 4% нейронов. Но головной мозг уникален, поскольку умеет «включать» своеобразные компенсаторные механизмы, чтобы сохранять нормальную работу нервной системы.
Если же потенциалы компенсации иссякли, а вместе с этим экстрапирамидная система (в ее состав входит черное вещество и пр.) лишилась 80% нейронов, возникают типичные для болезни Паркинсона симптомы. То есть, в анормальном положении разрушение соответствующего вида нейронов происходит активнее. И чем старше человек, тем выше вероятность достижения порогового уровня. Медики выдвигают гипотезу, что заболевание связано с увеличением продолжительности жизни, так как недуг преимущественно одолевает лиц пожилой группы.
Более интенсивное уменьшение числа нейронов, чем при нормальной физиологии старения, при болезни Паркинсона начинается задолго до проявления основных симптомов. И только спустя десятилетия человек, достигнув пожилого возраста, понимает, что болен.
Конкретно БП относят к идиопатической форме, что говорит о самостоятельной (первичной) болезни, которая возникает по необъяснимым причинам. Отсюда следует, что она не связана с генетическими факторами или какими-либо другими заболеваниями. При обследовании пациента врачи не могут установить этиологию ее развития.
В медицине существует еще один термин – «паркинсонизм». Паркинсонизм – обобщающее понятие, характеризующее в целом синдром, что связан с поражениями экстрапирамидной системы первичного или вторичного генеза. В отличие от первичной формы (истинной БП), вторичный паркинсонизм имеет первопричину, которая ведет к такому же клиническому исходу. Первопричинами вторичного паркинсонизма могут быть:
Основываясь на клинические данные, в 3/4 случаев синдрома паркинсонизма выявляют именно болезнь Паркинсона, то есть, идиопатическую (включая ювенильную) форму.
Статистика заболеваемости
По частоте развития среди нейродегенеративных патологий БП занимает второе место после болезни Альцгеймера. По данным ВОЗ, болезнь довольно распространена повсеместно: всего в мире насчитывается более 6 млн. людей с таким сложным диагнозом. Уровень заболеваемости по России соответствует 140-160 случаям на каждые 100 тыс. населения. При этом из года в год неуклонный рост прослеживается в распространении патологии даже среди молодых людей в возрасте 30-40 лет. Согласно статистике, каждый 10-й пациент не старше 40 лет. Если дебют БП приходится на любые годы до 40 лет, ее называют ювенильным паркинсонизмом.
На основании предоставленной информации разными авторами, до 55 лет риски заболеваемости в среднем составляют 0,5%, от 55-74 лет – 1,5%, 75-85 лет – 2,5-3%, старше 85 лет – 4-4,5%. Наиболее уязвимый к заболеванию контингент людей – мужчины. Инвалидизация, как правило, наступает спустя 3-5 лет с момента манифестации симптомов. Средний показатель выживаемости – 15 лет. Болезнь Паркинсона относится к числу заболеваний с относительно невысокими цифрами летальности. Причинами смертельных исходов преимущественно являются осложнения после падения, инфекции легких, ТЭЛА, инфекционный патогенез мочевыводящих путей.
Симптомы болезни Паркинсона: от ранних до поздних
Диагностика болезни Паркинсона на ранней стадии сопряжена большими трудностями. Ранняя симптоматика либо вообще отсутствует, либо характеризуется неспецифическими проявлениями, которые могут не восприниматься людьми за серьезную проблему. К числу первых симптомов, которые могут иметь связь с паркинсонизмом, относят:
Клиницисты объясняют развитие таких состояний, предшествующих явным двигательным расстройствам, вовлечением при стартовавшей нейродегенерации значительного количества нервных структур. Заболевание от предсимптомной до симптомной стадии проходит в несколько патоморфологических этапов.
Далее морфологические нарушения продолжаются, и, начиная с 4 этапа, когда дефицит дофамина составит 60%-80%, открываются клинические симптомы. Их спектр достаточно разнообразен, однако наиболее специфичными проявлениями паркинсонизма являются:
Диагностика и лечение болезни Паркинсона
Врачи говорят, что, если выявить и начать лечить патологию еще на ранней стадии (в момент самого начала гибели нейронов), можно было бы притормозить скорость разрушающего процесса и не допустить порогового уровня. Так, человек и в 100 лет не ощутил бы признаков заболевания. Но вся беда в том, что вряд ли кто пойдет к врачу в отсутствие проблем. Пациенты обращаются, когда появляются симптомы, но вот с резервами то нейронов уже катастрофа, их почти не осталось, что делает невозможным достижение такого перспективного плана.
В неврологической практике встречается еще одна проблема диагностики: неврологи часто допускают ошибки в установлении диагноза, игнорируя принципы дифференциации и комплексности. Отсюда возникают грубейшие просчеты в назначении симптоматического пособия, пациент получает зачастую неадекватную терапию, порой, в неоправданно поздние сроки. Многих попросту лечат не от той болезни, что есть по существу на самом деле. Либо рекомендуют лекарства и дозы, не соответствующие стадии патогенеза, возрасту пациента, сопутствующим патологиям, роду профессии и т. д. В результате клиническое состояние доходит до критической фазы, из-за чего часто требуется нейрохирургическая помощь, то есть, операция на головном мозге.
Врач обязан провести глубокую оценку моторных, рефлективных, психических расстройств, затем досконально дифференцировать признаки болезни. Однако и этого мало, ведь аналогичная клиника нередко присутствует при других патологиях и синдромах. Например, при гидроцефалии, опухолях мозга, депрессиях, истерии, кататоническом ступоре, синдроме Исаакса, эссенциальном треморе, пр. После осмотра окончательно и достоверно определить, имеет ли место паркинсонизм и какие структуры параллельно страдают, сможет уже только патоморфологическое исследование мозга.
Прием нейрохируга: изучение данных томографии мозга
Болезнь Паркинсона – пожизненная патология, полностью избавить от нее невозможно. Больному для улучшения качества жизни могут быть назначены в отдельном виде или в комбинации лекарства-симптоматики:
Принцип действия лекарственных средств направлен на коррекцию нарушенного биохимического баланса в базальных ядрах, восполнение недостающих веществ. В итоге, пока их пациент принимает, симптомы устраняются или становятся менее выраженными. После их отмены происходит быстрое возвращение симптомов с тенденцией стремительной прогрессии. Лекарства имеют многообразный спектр противопоказаний и ряд тяжелых побочных эффектов, поэтому должны выбираться очень осторожно хорошим специалистом по неврологии.
Хирургическая операция при болезни Паркинсона
В современной мировой практике для лечения болезни Паркинсона активно применяются хирургические методы. Операции позволяют существенно сгладить симптоматику, поспособствовать заметному улучшению уровня качества жизни. Обратиться к перспективной нейрохирургии иногда очень даже целесообразно. Особенную важность они представляют при предполагаемо продолжительном сроке жизни и крайне неудовлетворительном состоянии. Перечислим все показания, когда проблему уместно решать оперативно:
Операции по поводу симптомов болезни Паркинсона имеют противопоказания к назначению. В оперативном вмешательстве может быть отказано, если:
В нейрохирургическом арсенале для лечения больных с диагнозом «паркинсонизм/болезнь Паркинсона» применяются стереотаксические методики с доказанной эффективностью, это:
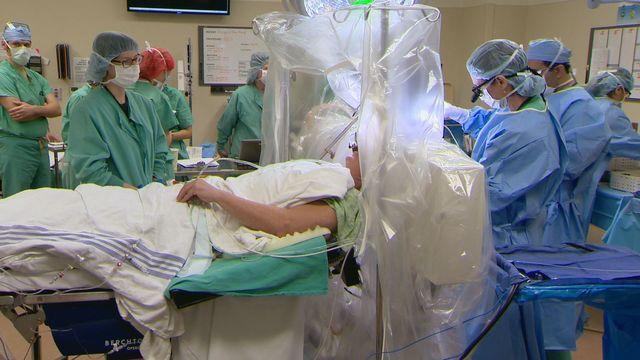
Во время хирургической операции
Главный принцип хирургического лечения базируется на локальном разрушении подкорковых ядер головного мозга, что ответственны за появление дрожательного синдрома и ригидности мышц. Такие операции в значительной мере позволяют пациентам адаптироваться к условиям повседневной жизни, ведь некоторым не под силу даже выполнить элементарные действия – поднести ко рту ложку, поставить подпись, застегнуть пуговицу.
Пройдя нейрохирургическое вмешательство, пациентам, и это первостепенно значимо, возвращаются способности к самостоятельному обслуживанию. Очередной веский аргумент в пользу хирургической терапии – это возможность перейти на самые низкие, неагрессивные лекарственные дозы. Хирургия во многих случаях делает жизнь полноценной или максимально приближенной к норме здорового человека.
Рассмотрим же, что представляют собой все тактики операций, которые спасают людей от тех злостных мучений, уготованных болезнью Паркинсона.
Процедура таламотомии
Таламотомия – стереотаксический прием нейрохирургии, в момент которого оказывается точечное деструкционное воздействие на отдельные ядра и проводящие пути таламуса. Процедура выполняется под местным наркозом, человек остается в сознании и полном контакте с врачом. После обезболивания голова закрепляется в стереотаксической раме. Далее в черепной коробке делается 1,5-саниметровое отверстие, через которое к таламусу под КТ-контролем подводится зонд-электрод. При подаче электротока кончик зонда нагревается до 75-80 градусов, что вызывает абляцию (прижигание) интересующих нервных структур. После вмешательства на череп накладывается стерильная повязка.
Деструкция таламусной области эффективна только при контрлатеральном (одностороннем) треморе. Процедура сложная, долгая (манипуляции занимают до 2 часов), по степени инвазивности средняя. Она показывает в 90% случаев хорошие и отличные результаты. После таламотомии достигается устойчивый и длительный противотреморный эффект, у большинства он отмечается сразу в операционной. Осложнения случаются не сильно часто, у 2% пациентов. Послеоперационные нарушения в основном представлены расстройствами чувствительности и психики, односторонними парезами.
Видео на английском языке, но весьма наглядное:
Операция паллидотомия
Суть паллидотомии заключается в деструкции медиальной части бледного шара с целью подавления его гиперактивности. Бледный шар головного мозга отвечает за регуляцию мышечного тонуса и двигательных способностей. При его чрезмерной активности, как в случае с паркинсонизмом, возникает неадекватное воспроизведение движений. Процедура позволяет пресечь его патологическую импульсацию, которая провоцирует торможение нервных клеток таламуса и моторных областей коры головного мозга.
Эта операция сходна с таламотомией, отличие – функциональная область для прямого нанесения деструкции. Этот способ может быть рассмотрен в качестве лечения дискинезий от приема леводопы, сочетающихся с болезненным спазмированием мышц. Улучшение при таких дискинезиях наступает в 90% случаев, ригидность и брадикинезию сократить удается в 80%, тремор – только в 50-55%. Безусловно, если операция была проведена безупречно. Однако если у пациента ведущим симптомом выступает тремор, проводить паллидотомию неуместно, предпочтительнее таламотомия.
Хирургический шов после процедуры.
В ходе манипуляций на бледном шаре крайне важно использовать самые щадящие интраоперационные системы деструкции (например, криозонды) для столь уязвимого участка.
По причине близкого расположения зрительного тракта и внутренней капсулы, индивидуальной вариабельности размеров БШ от паллиодотомии в ведущих клиниках мира все чаще стали отказываться. Методика сопряжена высокими рисками необратимых последствий: выпадением полей зрения, внутримозговыми кровоизлияниями, дизартриями и др.
Метод глубокой стимуляции мозга
Уникальная методика Deep Brain Stimulation, изобретенная в 80-х годах французскими специалистами, стала хорошей альтернативой таламо- и поллидотомии. Техника ее проведения состоит во вживлении электродов в мозг. Они будут обеспечивать должный контроль над тремором, скованностью и замедленностью движений, распознавая и блокируя аномальные сигналы ЦНС. Эта процедура нейростимуляции не подойдет пациентам с немоторными нарушениями.
Миниинвазивный сеанс осуществляется в 2 этапа. На первом этапе под местной анестезией через крошечное отверстие в черепе в зону субталамического ядра вводятся специальные электроды. Для высокоточного и безопасного внедрения электродов используется трехмерная КТ-навигация. Свободные концы электродов оставляют под кожей головы. В течение примерно 1 недели импланты тестируются и настраиваются посредством магнитных приборов. По достижении необходимого эффекта переходят ко второму этапу.
На втором этапе выполняется имплантация импульсного генератора под кожу, немного ниже ключицы. Концы электродов соединяют с генератором электроимпульсов, затем на область рассечения кожи накладывается косметический шов. После окончания вмешательства выполняется контрольная проверка работы установленной системы. Первое время в месте операции могут беспокоить болезненные явления, которые постепенно сойдут на нет. В целом процедура переносится относительно легко и редко осложняется последствиями. Выраженность тремора сокращается, как показывают наблюдения, во многих случаях на 85% и более.
При выписке больному выдается специальный пульт магнитного действия, которым можно будет выключить или включить основное устройство. В случае усиления симптомов, врач изменит настройки нейростимулятора, используя только внешние источники управления. Стимулятор работает от батарей, срок службы которых составляет 5 лет и более, самые последние модели рассчитаны на срок эксплуатации до 10 лет.
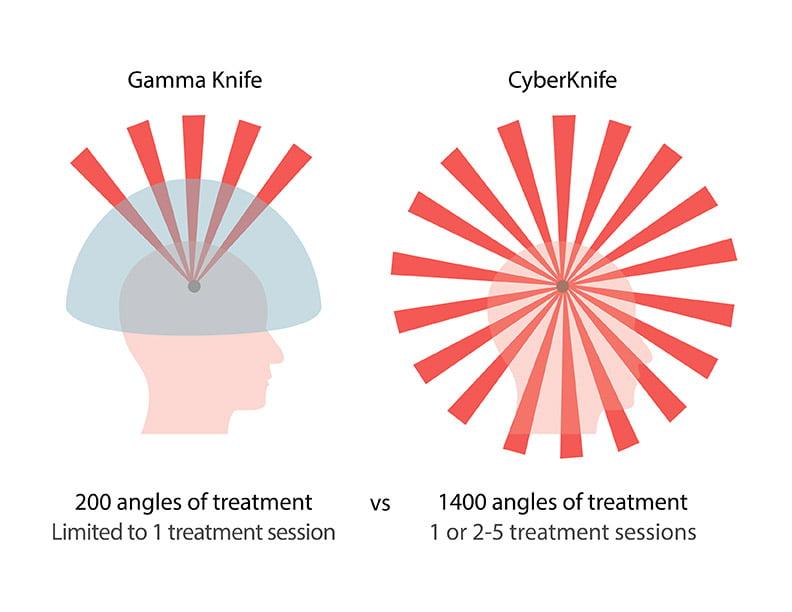
Радиохирургия на Гамма-ноже, Кибер-установках
Радиохирургические операции на Гамма и Кибер ножах приобрели грандиозный успех в нейрохирургическом мире. Такие процедуры безопасны, безболезненны и бескровны, поскольку проводятся без вовлечения методов трепанации и разрезов, не требуют прямого контакта хирургических инструментов с тканями головного мозга. Пациента не нужно госпитализировать, сеанс проходит в амбулаторных условиях. По терапевтической мощи передовые технологии не уступают, а иногда даже превосходят классические операции.
Гамма-нож и Кибер-нож – «золотой стандарт» современной радиохирургии. С их помощью всего за 1 сеанс устраняются очаги, вызывающие клинику болезни Паркинсона. Работают методики по принципу прицеленного воздействия радиоактивным потоком лучей на патологическую область, к примеру, на таламус или бледный шар. В участки, которые виновны в появлении дрожательного синдрома и других нарушений, поступает концентрированная доза радиации. Под действием радиоактивной энергии облучаемый объект разрушается и обезвреживается, а вслед за этим наступает облегчение для пациента.
За процессом посредством компьютерного оборудования будет следить врач из соседнего кабинета. Облучения бояться не стоит, «умные» установки работают только в изолированном поле, четко в избранной точке. Поэтому они не окажут негативного влияния на организм и близлежащие структуры головного мозга. Пациенту нужно просто от 30-60 минут полежать на столе установке. А уже через час после проведенной терапии он сможет покинуть лечебное учреждение, на следующий день вернуться к повседневной деятельности. Эффективность лечения тремора на системе Гамма- или Кибер-нож составляет 95% и более.
Профильные клиники
В Европе одним из лидеров в области нейрохирургического лечения и реабилитации пациентов с диагнозом болезни Паркинсона является Чехия. Чехия имеет огромный опыт в восстановлении опорно-двигательных функций и утраченного потенциала ЦНС не только при паркинсонизме, но и при болезни Альцегеймера, эпилепсиях, мозговых новообразованиях. Медицинская помощь предоставляется по современным стандартам нейрохирургии.
Чешские специалисты практикуют исключительно проверенные, действенные и щадящие технологии, актуальные нынешнему времени. Клиники Чешской Республики – учреждения с мировым именем, которые не уступают медучреждениям Германии и Израиля. И при этом цены на радио- и нейрохирургическую помощь при паркинсонизме в Чехии в разы доступнее (не менее чем в 1,5 раза ниже), чем в этих странах.
Как узнать паркинсона болезнь
1 Российская медицинская академия последипломного образования;
2 Центр экстрапирамидных заболеваний (Москва);
3 Кабинет экстрапирамидных расстройств Приморской краевой клинической больницы №1 (Владивосток)
Болезнь Паркинсона (БП) – прогрессирующее нейродегенеративное заболевание, характеризующееся сочетанием гипокинезии с мышечной ригидностью и/или тремором покоя, а также с позднее развивающейся постуральной неустойчивостью и широким спектром немоторных нарушений, включая вегетативные, психические, диссомнические и сенсорные симптомы. В качестве основного звена патогенеза БП рассматривается формирование нейротоксических агрегатов небольшого пресинаптического белка альфа-синуклеина (основного компонента телец Леви) сопровождающееся гибелью пигментированных нейронов вентролатеральных отделов компактной части черной субстанции. Однако в последние годы установлено, что с поражением черной субстанции коррелируют лишь основные двигательные симптомы паркинсонизма, в то же время дегенеративный процесс при БП вовлекает и другие группы нейронов в различных зонах головного мозга, а также и в периферической нервной системе, что лежит в основе многочисленных немоторных проявлений болезни [1, 3].
Эпидемиология
По данным сплошного популяционного исследования, распространенность БП в России составляет 139 случаев на 100 000 населения, заболеваемость БП – 16 случаев на 100 000 населения в год. С увеличением возраста риск БП увеличивается, и выявляемость БП среди лиц старше 65 лет составляет уже около 1%. Большинство случаев заболевания возникают в возрасте 60–70 лет. Однако в 15% случаев БП дебютирует в возрасте до 45 лет.
Исходя из имеющихся данных и половозрастной структуры населения России, можно примерно оценить общую численность больных с БП в нашей стране в 210 тысяч, при этом ежегодно заболевание возникает примерно у 20 тысяч пациентов. Ориентировочные расчеты показывают, что, как минимум, четверть пациентов (то есть более 50 тысяч) оказываются вне сферы медицинской помощи, причем в большинстве своем это пациенты с ранней стадией заболевания [3].
Диагностика
Диагноз БП проводится в 2 этапа. На первом (синдромальном) этапе синдром паркинсонизма требуется отличить от других состояний, имитирующих его (таблица 1).
Таблица 1. Состояния, требующие дифференциальной диагностики с паркинсонизмом.
| При наличии тремора | В отсутствие тремора |
| Усиленный физиологический тремор Гепатолентикулярная дегенерации | Апатико-абулический синдром Деменция с феноменом паратонии (противодержания) Кататония |
Ключевое значение в дифференциальной диагностике имеет выявление признаков гипокинезии. Начальные симптомы гипокинезии могут характеризоваться затруднениями при письме, нажатии кнопок на пульте, чистке зубов, печатании на клавиатуре, доставании мелких предметов, например, монет из сумки или кармана, надевании тапочек и т.д. Иногда уже на ранней стадии проявляется слабость и отставание одной из ног при ходьбе с изменением привычного рисунка походки. Характерно ослабление содружественных движений рук при ходьбе (ахейрокинез), нарушение подзарядки часов («симптом ролекса»). Могут обратить внимание ослабление голоса, замедление, ослабление интонирования или нечеткость речи (особенно при быстром произнесении морфологически сложных слов). При осмотре для выявления гипокинезии пациента просят выполнить определённые движения в течение примерно 20 секунд в максимально быстром темпе и с максимальной амплитудой. При этом врачу следует обращать внимание на замедленную инициацию движения, асимметрию движений, но главное – на особую форму истощаемости движений (декремент), которые по мере повторения все более замедляются, уменьшаются по амплитуде, требуют от пациента все больших усилий. Феномен истощаемости может выявляться при всех оцениваемых движениях, но иногда отмечается только в одном из тестов. Следует учитывать, что замедленность и неловкость движений, характерные для пациентов с паркинсонизмом, на ранней стадии можно спутать с проявлениями пирамидной и мозжечковой недостаточности, а также тяжелой депрессии, однако для этих состояний не характерен декремент движений по мере их повторения. Следует учитывать, что гипокинезию бывает трудно выявить на фоне грубого тремора в конечности, однако и в этом случае важно не пропустить диагностически значимый феномен: при паркинсонизме после выполнения теста на гипокинезию пациент часто держит руку в фиксированной напряженной позе и не способен быстро расслабиться.
Ригидность мышц проявляется устойчивым (в отличие от спастичности) сопротивлением пассивным движениям в лучезапястных, локтевых, плечевых, коленных суставах, а также в шее, а субъективно – скованностью и неприятными болезненными ощущениями в конечностях. У части пациентов при проверке тонуса выявляется феномен «зубчатого колеса». Следует отличать ригидность от феномена противодержания (gegenhalten), характерного для пациентов с деменцией и поражением лобных долей. Противодержание быстро меняется в зависимости от направления и скорости пассивного движения.
Медленный (3–4 Гц) тремор покоя в одной руке или ноге – одно из частых начальных проявлений паркинсонизма. Наличие классического тремора покоя по типу «скатывания пилюль» или «счета монет» наиболее характерно для БП. Для выявления латентного тремора пациента просят совершать движения другой рукой, походить, выполнить задачу на отвлечение (например, отнимать от 100 по 7). Для выявления тремора в ноге нужно осмотреть пациента в положении сидя или лежа. Вместе с тем, в отсутствие гипокинезии тремор покоя не позволяет диагностировать ни паркинсонизм, ни БП. Следует учитывать, что, с одной стороны, в покое может наблюдаться эссенциальный и дистонический тремор, с другой стороны, при БП часто наблюдается постуральный и кинетический тремор.
Начальным проявлением БП, особенно у лиц молодого возраста, может быть дистония стопы, появляющаяся или усиливающаяся при ходьбе, значительно реже – дистония иной локализации.
Ранние немоторные нарушения. Начиная с самой ранней (продромальной) стадии заболевания пациента могут беспокоить эмоциональная угнетенность, повышенная раздражительность, быстрая утомляемость или ощущение постоянной усталости, а также такие вегетативные нарушения, как расстройства потоотделения («дефектный термостат»), например, профузное потоотделение в холодную погоду, а также склонность к запорам, учащенные и/или императивные мочеиспускания, усиленное слюнотечение в ночное время (симптом «мокрой подушки»), эректильная дисфункция. Гипоосмия часто возникает уже на премоторной стадии БП, однако редко привлекает внимание самого пациента, и для ее выявления необходимо формализованное исследование (с помощью специальных методик, например, обонятельного теста Пенсильванского университета – UPSIT). Важное диагностическое значение может иметь выявление признаков синдрома нарушения поведения во сне с быстрыми движениями глаз (тревожные сновидения, вокализации, сноговорение, движения, отражающие содержание сновидений), которые могут опережать другие проявления заболевания на многие годы. Указанные немоторные проявления могут повышать точность диагноза, основывающегося на ранних моторных симптомах болезни.
Дебютными проявлениями БП бывают также хронические болевые синдромы, чаще всего в спине и плечелопаточной области, связанные с повышенным мышечным тонусом, ограничением мобильности и постуральными нарушениями.
Уже на ранней стадии могут выявляться признаки умеренного когнитивного расстройства, в частности неустойчивость внимания и замедленность мышления, трудности поиска слов (феномен «кончика языка»).
«Красные флажки». Второй этап – этап нозологической диагностики – сводится к дифференциальной диагностике БП с другими нозологическими формами паркинсонизма. Он требует клинической оценки анамнестических данных и данных, выявляемых при неврологическом осмотре. Важное значение имеет выяснение лекарственного анамнеза. Такие препараты, как метоклопрамид, вальпроат натрия, циннаризин, амиодарон, могут быть причиной лекарственного паркинсонизма. Отмена препарата, спровоцировавшего развитие паркинсонизма, может не приводить к немедленному регрессу симптомов. Иногда после отмены «виновного» препарата и кратковременного улучшения состояние вновь ухудшается, что указывает на скрыто развивающийся дегенеративный процесс, который был «демаскирован» побочным действием лекарственных средств.
При неврологическом осмотре могут выявляться симптомы, атипичные для БП, требующие исключения иных заболеваний, вызывающих синдром паркинсонизма. Среди них можно выделить: симметричность, быстрое прогрессирование симптоматики с ранней утратой способности к передвижению в течние 5 лет, раннее развитие постуральной неустойчивости с падениями, отсутствие стойкого положительного эффекта адекватных доз препаратов леводопы, раннее развитие вегетативной недостаточности, быстрое присоединение деменции (в течении 1-го года), ограничение подвижности глазных яблок (особенно парез взора вниз), раннее развитие тяжелых псевдобульбарных синдромов, аксиальная дистония, пирамидные и мозжечковые знаки, наличие очаговых нарушений корковых функций.
Дополнительные методы исследования
В настоящий момент нет методов лабораторного или инструментального исследования, которые были бы обязательны у каждого пациента с подозрением на БП. В последние годы больным с БП часто проводят КТ или МРТ головного мозга, однако чаще всего в этом нет необходимости, и в большинстве случаев диагноз может быть установлен на основе клинических данных. Тем не менее, если клиническая картина у больного с синдромом паркинсонизма отклоняется от классического варианта, свойственного БП, в частности, отсутствует типичная реакция на дофаминергические средства, – необходимо проведение нейровизуализации.
При начале заболевания до 50 лет важно исключить гепатолентикулярную дегенерацию, о которой могут свидетельствовать роговичное кольцо Кайзера–Флейшера, низкий уровень церулоплазмина, повышение интенсивности сигнала от базальных ганглиев и мозжечка на Т2-взвешенных МРТ изображениях, повышенная экскреция меди с мочой.
Диагностическую значимость может иметь и транскраниальная сонография глубинных структур мозга, выявляющее при БП гиперэхогенные изменения в проекции черной субстанции, связанные с накоплением железа и установленные в 92% случаев клинически вероятной БП, однако его результаты можно интерпретировать лишь в клиническом контексте.
Из практически важных, но пока отсутствующих в нашей стране, методов диагностики следует упомянуть позитронно-эмиссионную томографию (ПЭТ) и однофотонную эмиссионную компьютерную томографию (ОФЭКТ), позволяющие изучить синаптическую передачу на всех уровнях, а также проводить мониторинг патологического процесса. При выявлении снижение накопления F18-флюородопы при ПЭТ и β-CIT при ОФЭКТ в полосатом теле можно говорить о вовлечении в патологический процесс пресинаптических нигростриарных терминалей (первичный паркинсонизм). Определение снижение накопления 11С-раклоприда (лиганд D2рецепторов) при ПЭТ будет указывать на уменьшение количества дофаминовых рецепторов в полосатом теле (паркинсонизм «плюс»).
Общие принципы начала лечения
Поскольку на данный момент способность замедлять процесс дегенерации за счет нейропротективного эффекта (возможность защищать интактные клетки от повреждения) или нейрорепаративного эффекта (возможность восстанавливать активность частично поврежденных клеток) ни у одного из применяющихся средств убедительно не доказана, лечение основывается пока на симптоматическом действии. Тем не менее потенциальная возможность нейропротективного эффекта, подтверждаемая экспериментальными или клиническими данными, должна учитываться при назначении лечения.
В настоящее время широкое распространение получила концепция, подчеркивающая важность раннего назначения дофаминергической терапии – немедленно после установления диагноза – с тем, чтобы быстрее скорректировать нейрохимический дисбаланс в мозге и поддержать процессы компенсации.
Если ранее подчеркивалась необходимость возможно более длительного сохранения монотерапии, то в настоящее время преимущества такого подхода не представляются очевидными – по сравнению с ранним переходом к комбинации средств с разным механизмом действия. Вопрос о необходимости монотерапии или комбинированной терапии должен решаться индивидуально. В любом случае при выборе препаратов и их дозы следует стремиться не к полному устранению симптомов, а к существенному улучшению функций, позволяющему поддерживать бытовую и профессиональную активность. В то же время следует избегать внесения в схему лечения сразу нескольких изменений (например, повышения дозы сразу нескольких средств или добавления сразу нескольких препаратов), это позволяет оценить отдельно эффективность и безопасность каждого из назначаемых средств.
Принципы выбора противопаркинсонического препарата
Выбор препарата на начальном этапе лечения проводят с учетом возраста, выраженности двигательного дефекта, трудового статуса, состояния нейропсихологических функций, наличия сопутствующих соматических заболеваний, индивидуальной чувствительности пациента. Помимо достижения оптимального симптоматического контроля, выбор препарата определяется необходимостью отсрочить момент развития моторных флуктуаций и дискинезий (таблица 2).
Таблица 2. Выбор препарата для начального лечения болезни Паркинсона.
| Препараты | Возможность использования в качестве средства первого выбора | Степень симптоматического улучшения | Нейро-протективный потенциал | Риск побочного действия | |
| Флуктуации и дискинезии | Другие побочные эффекты | ||||
| Леводопа | + | +++ | +? | ↑ | ↑ |
| Агонисты дофаминовых рецепторов | + | ++ | +? | ↓ | ↑ |
| Ингибитор МАО В | + | + | +? | ↓ | ↑ |
| Амантадин | + | + | +? | ↓ | ↑ |
| Холинолитики | — | + | — | ? | ↑ |
У лиц моложе 50 лет при легкой или умеренной выраженности двигательных нарушений в отсутствие выраженных когнитивных нарушений назначают один из следующих препаратов: агонист дофаминовых рецепторов, ингибитор моноаминооксидазы типа В, амантадин. При более легком двигательном дефекте может быть назначен ингибитор МАО В, при более выраженном дефекте предпочтительнее начинать с лечения с одного из агонистов дофаминовых рецепторов. Неэрголиновые агонисты (например, прамипексол, ропинирол, ротиготин или проноран) ввиду более благоприятного профиля побочных эффектов предпочтительнее, чем эрголиновые (бромокриптин, каберголин). При недостаточной эффективности или плохой переносимости одного из агонистов дофаминовых рецепторов может быть испробован другой агонист дофаминовых рецепторов или препарат другой фармакологической группы. Рациональна комбинация агониста дофаминовых рецепторов, ингибитора МАО типа В и амантадина, к которой следует переходить постепенно, добавляя препарат новой группы, если ранее назначенное средство не обеспечило ожидаемого эффекта.
Антихолинергические средства (например, бипериден) показаны при наличии выраженного тремора покоя либо болезненной дистонии при условии сохранности нейропсихологических функций. Их целесообразно добавлять к комбинации агониста дофаминовых рецепторов с ингибитором МАО В и/или амантадином, если она у пациента относительно молодого возраста не обеспечила подавления тремора в той степени, в которой это необходимо для поддержания его трудоспособности.
Если указанные препараты в максимально переносимых дозах и их комбинация не обеспечивают адекватного состояния двигательных функций и социальной адаптации больных, назначают препарат леводопы в минимальной эффективной дозе [4].
У лиц в возрасте 50–70 лет при умеренном двигательном дефекте и относительной сохранности когнитивных функций лечение начинают с ингибитора МАО типа В (при легких симптомах паркинсонизма) или одного из агонистов дофаминовых рецепторов. В дальнейшем целесообразен постепенный переход к комбинации агониста дофаминовых рецепторов, ингибитора МАО типа В и амантадина (при условии хорошей переносимости). Больным после 60 лет антихолинергические средства, как правило, не следует назначать из-за риска ухудшения познавательных функций и других побочных эффектов. При недостаточной эффективности комбинации указанных выше препаратов добавляют препарат леводопы в минимальной эффективной дозе (200–400 мг в сутки).
У лиц в возрасте 50–70 лет при выраженном двигательном дефекте, ограничивающем трудоспособность и(или) возможность самообслуживания, а также при наличии выраженных когнитивных нарушений и необходимости получения быстрого эффекта лечение начинают с препаратов, содержащих леводопу. Если небольшие или средние дозы леводопы (300–500 мг леводопы в сутки) не обеспечивают необходимого улучшения, к ним последовательно могут быть добавлены агонист дофаминовых рецепторов, амантадин и ингибитор МАО В.
У пожилых лиц (старше 70 лет), особенно при наличии выраженного когнитивного снижения и соматической отягощенности, лечение следует начинать с препаратов леводопы. Указанные возрастные границы относительны, и общий принцип скорее заключается в том, что чем моложе больной, тем позже следует вводить препараты леводопы. Кроме того, решающее значение играет не столько хронологический, сколько биологический возраст больных.
Применение препарата прамипексола с длительным высвобождением на ранней стадии БП
Разработка новых лекарственных форм противопаркинсонических препаратов, обеспечивающих их длительное высвобождение и допускающих однократный прием в течение дня, не просто делает лечение более удобным, но и, улучшая приверженность пациентов лечению, повышает долгосрочную эффективность терапии. Кроме того, при медленном высвобождении препарата в течение суток достигается более стабильная его концентрация в крови, что может обеспечить его лучшую переносимость и эффективный контроль симптомов заболевания в течение всего дня (как в дневное, так и в ночное время).
Новая лекарственная форма прамипексола с длительным (контролируемым) высвобождением, предполагающая однократный прием в течение дня, применяется в европейских странах и США с 2009 года, а в нашей стране – с 2012 года. Она представляет собой матриксную таблетку, в которой активное вещество равномерно распределено в полимерном матриксе. В желудочно-кишечном тракте матрикс впитывает жидкость и превращается в гель, который равномерно высвобождает прамипексол в течение 24 ч. Поскольку прамипексол хорошо растворяется в жидкой среде, независимо от ее pH, активное вещество высвобождается из матрикса и всасывается на протяжении всего кишечника. Скорость опорожнения желудка и моторика кишечника не оказывают существенного влияния на действие препарата. Параметры всасывания не зависят также от того, принимается препарат натощак или после еды [2].
При разработке новой лекарственной формы была учтена возможность простого, одномоментного перехода от традиционной формы препарата к новой. Условием этого является то, что равные суточные дозы препарата с немедленным высвобождением (принимаемым 3 раза в день) и длительным высвобождение (принимаемым 1 раз в день) оказывают одинаковое противопаркинсоническое действие. Различие между новой и традиционной лекарственными формами прамипексола заключается лишь в скорости высвобождения активного вещества. Период полужизни прамипексола при применении обеих форм один и тот же, но благодаря контролируемому высвобождению обеспечивается более длительное поддержание терапевтической концентрации препарата в крови [5].
Эквивалентность действия равных суточных доз препаратов прамипексола с немедленным и длительным высвобождением была подтверждена в целом ряде клинических испытаний.
Следует подчеркнуть особое удобство новой лекарственной формы прамипексола, которую достаточно принимать один раз в день, для пациентов с ранней стадией БП, продолжающих работать. Во избежание побочного действия препарат назначается путем медленного титрования – по той же схеме, что и препарат с немедленным высвобождением. Для этого таблетки прамипексола с длительным высвобождением выпускаются в нескольких дозировках: 0,375, 0,75, 1,5, 3 и 4,5 мг. Лечение начинают с дозы 0,375 мг 1 раз в день, далее при условии хорошей переносимости каждые 7 дней переходят на следующий уровень дозы до достижения оптимального эффекта, максимально до 4,5 мг/сут (таблица 3). После достижения дозы 1,5 мг/сут титрование иногда целесообразно проводить медленнее, так как развитие полного лечебного эффекта может требовать нескольких недель. Рекомендуемая доза для поддерживающей терапии (как на ранней, так и на развернутой или поздней стадиях заболевания) может колебаться от 0,375 до 4,5 мг/сут. Наиболее часто применяемая доза – 3 мг/сут.
Таблица 3. Схема титрования прамипексола с длительным высвобождением.
| Неделя | Доза |
| 1-я | 0,375 мг 1 раз в день |
| 2-я | 0,75 мг 1 раз в день |
| 3-я | 1,5 мг 1 раз в день |
| 4-я | 2,25 мг 1 раз в день |
| 5-я | 3 мг 1 раз в день |
| 6-я | 3,75 мг 1 раз в день |
| 7-я | 4,5 мг 1 раз в день |
Лекарственные средства, эффективность которых при БП не доказана
В клинической практике широко применяют лекарственные средства, эффективность которых при БП не доказана и которые, следовательно, не могут быть рекомендованы к применению при этом заболевании. Прежде всего, к ним относятся так называемые ноотропные, нейрометаболические и вазоактивные препараты. Возможно, некоторые из этих средств оказывают определенное лечебное действие, но прежде, чем рекомендовать конкретный препарат, следует провести адекватную оценку его эффективности. Специалисты, занимающиеся лечением БП, прекрасно знают, что определенная часть больных хорошо реагирует на плацебо, причем этот эффект оказывается нестойким. Соответственно, затраты на подобное лечение оказываются бессмысленными.