Урок 7. Понятие об окислительно-восстановительных реакциях
При изучении строения атома, описании свойств некоторых элементов, химической связи неоднократно упоминалось о том, что атомы принимают или отдают электроны. Очевидно, существуют химические реакции, в ходе которых одни атомы отдают электроны другим атомам, которые их принимают.
Процесс отдачи электронов называется окислением, а процесс приёма электронов — восстановлением. Оба процесса происходят одновременно, так как не могут отданные электроны исчезнуть в «никуда» — должна существовать частица, которая их присоединит, и наоборот. Поэтому процессы окисления и восстановления, протекающие одновременно, называются окислительно-восстановительными реакциями. При этом атом*, отдающий электроны, называется восстановителем, а атом, принимающий электроны, — окислителем.
* В окислительно-восстановительной реакции участвует реальная частица, входящая в понятие химического элемента, — атом, ион, радикал.
Что же происходит с такими атомами? Пусть атом меди в каком-то процессе отдаст два электрона:
Если эта реакция происходит в растворе, то можно увидеть, как жёлто-красный металл медь уменьшится в размерах, а раствор приобретает голубую окраску, характерную для ионов меди. Очевидно, что свойства исходного простого вещества, состоящего из атомов, и полученных ионов — различно.
Этот же процесс может происходить и при окислении меди кислородом:
Но ионов здесь не образуется, хотя признак реакции (изменение цвета) налицо. В таких случаях изменение состояния окисленности обозначают при помощи степени окисления. Так, атому кислорода, который для завершения внешнего энергетического (электронного) уровня должен присоединить 2 электрона, почти во всех соединениях приписывают степень окисления –2. Поскольку молекула СuО электронейтральна — атом меди приобретает степень окисления +2.
Заметьте: заряд иона записывается так:
сбоку, сначала число, потом заряд (причём цифра 1 не пишется). Степень окисления записывают по-другому:
над символом элемента, сначала заряд, потом число (причём не только пишется цифра 1, но может быть даже дробное число).
Этой формой записи подчеркивают различие этих понятий:
Величины этих зарядов могут совпадать, но очень часто они различаются. Рассчитаем, например, степени окисления элементов в химической формуле, соответствующей серной кислоте. При этом степень окисления кислорода равна –2, а водорода +1 (так как он может отдать только один электрон):
Суммарный заряд двух атомов водорода равен +2, а четырёх атомов кислорода:
Видно, что для того, чтобы молекула была электронейтральна, не хватает положительных зарядов, следовательно, степень окисления серы в серной кислоте равна +6. (Такого иона серы вообще не существует!)
При расчёте степеней окисления следует руководствоваться следующими правилами:
1. Степень окисления атомов химических элементов в простом веществе равна нулю:
2. Степени окисления атомов металлов в соединениях всегда положительны и равны их валентности:
4. Степень окисления химических элементов в кислотном остатке соли такие же, как в соответствующей кислоте:
5. Алгебраическая сумма степеней окисления в любом соединении равна нулю.
Задание 7.1. Расставьте степени окисления химических элементов в соединениях:
Если вы испытываете затруднения при расстановке степеней окисления, рекомендуется составлять простейшие математические уравнения.
Известные степени окисления
Суммарные степени окисления: +2 + 2х –14 = 0 (математическое уравнение, которое решается относительно «х»)
х = 6, т. е. степень окисления атома хрома в этом соединении равна +6.
Определив степени окисления элементов в уравнении реакции, можно определить, какой атом является окислителем, какой — восстановителем:
Задание 7.2. Определите окислитель и восстановитель в уравнениях реакций:
Из этих примеров видно, что число электронов, принятых окислителем, может отличаться от числа электронов, отданных восстановителем. Но этого быть не должно(!), так как при этом нарушается закон сохранения материи. Значит, число отданных электронов должно равняться числу принятых электронов. А для этого следует изменить число атомов окислителя и восстановителя, поставив соответствующие коэффициенты. Например, в данном случае:
Эти коэффициенты (3 и 2) означают, что три атома меди отдают шесть электронов, а два атома азота принимают шесть электронов:
Или в краткой форме:
Теперь осуществлён баланс (равенство) электронов, поэтому именно эти коэффициенты из электронного баланса (3 и 2) должны быть в уравнении реакции
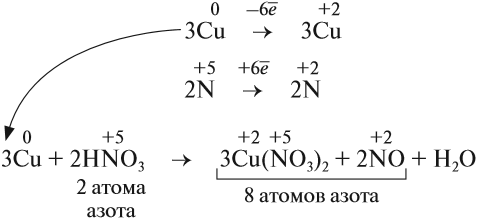
Но теперь не осуществляется баланс по азоту! Где же допущена ошибка? Дело в том, что в электронном балансе учитываются только электронные процессы окисления и восстановления, т. е. учитываются только те атомы, которые меняют степени окисления, а часть атомов не изменила ее:
Отсюда правило: коэффициенты электронного баланса ставят только к тем атомам, которые с данной степенью окисления встречаются в химическом уравнении один раз.
Исправим ошибку и уравняем атомы остальных элементов:
Проверим по кислороду:
Правила расстановки коэффициентов методом электронного баланса
1. Расставить степени окисления.
2. Выписать элементы, изменившие степени окисления, указав число отданных и принятых электронов. Определить окислитель и восстановитель.
3. Поставить дополнительные коэффициенты, уравняв число отданных и принятых электронов.
4. Проверить эти коэффициенты: они должны соответствовать числу атомов данного элемента в молекуле. Например, если дополнительный коэффициент нечётный, а в молекуле чётное число атомов (например, Сl2), то оба дополнительных коэффициента удваиваются.
5. Проверенные коэффициенты переносят в уравнение, считая атомы, к тем элементам, которые с данной степенью окисления встречаются в уравнении ОДИН раз.
6. Затем уравнивают атомы:
7. Проверяют по кислороду.
Рассмотрим эти правила на примере. Требуется уравнять (т. е. расставить коэффициенты в уравнении реакции):
1, 2, 3.
4. Поскольку число атомов хлора в молекуле чётное (2), а коэффициент к хлору нечётный (5), удвоим оба дополнительных коэффициента:
Обратите внимание, что перед молекулой хлора поставлен коэффициент 5, а не 10, так как нужно считать атомы хлора: 5 · 2 = 10 атомов.
6. Уравняем остальные атомы:
7. Атомы кислорода до и после реакции пересчитайте сами.
Задание 7.3. Уравнять методом электронного баланса:
Вы можете проверить степень усвоения материала этой главы, выполнив упражнения ЕГЭ из разделов 4, 28 и частично 36.
Выводы
Окислительно-восстановительные реакции (ОВР) — это процессы, в которых изменяются степени окисления атомов. Степени окисления атомов изменяются потому, что один атом (окислитель) принимает электрон от атома восстановителя. При этом число принятых и отданных электронов должно быть одинаковым. На этом основан метод электронного баланса, при помощи которого расставляют коэффициенты в уравнениях ОВР.
Окислительно-восстановительные реакции


Процессы, протекающие в природе и осуществляемые человеком, в большинстве своём представляют ОВР. Такие важнейшие процессы, как дыхание, обмен веществ, фотосинтез (6CO2+H2O = C6H12O6 + 6O2), — всё это ОВР.
В промышленности с помощью ОВР получают аммиак, серную, соляную кислоты и многое другое.
Восстановление металлов из руд — фактически основа всей металлургической промышленности — тоже окислительно-восстановительные процессы. Например, реакция получения железа из гематита: 2Fe2O3 + 3С = 4Fe+3CO2.
Окислители и восстановители: характеристика

Говорят, что окислители, принимая электроны, восстанавливаются, а восстановители — окисляются в процессе отдачи электронов.
Важнейшие представители окислителей и восстановителей представлены в следующей таблице:
| Типичные окислители | Типичные восстановители |
| Простые вещества, состоящие из элементов с высокой электроотрицательностью (неметаллы): йод, фтор, хлор, бром, кислород, озон, сера и т. п. | Простые вещества, состоящие из атомов элементов с низкой электроотрицательностью (металлы или неметаллы): водород H2, углерод C (графит), цинк Zn, алюминий Al, кальций Ca, барий Ba, железо Fe, хром Cr и так далее. |
| Молекулы или ионы, содержащие в составе атомы металлов или неметаллов с высокими степенями окисления:
Как определить, является атом окислителем или восстановителем: достаточно записать СО и понять, какие атомы её увеличили впроцессе реакции (восстановители), а какие уменьшили (окислители). Вещества с двойственной природой
При взаимодействии с восстановителем пероксид проявляет окислительные свойства, а с окислителем — восстановительные. Рассмотреть подробнее можно при помощи следующих примеров: 2KMnO4 + 5H2O2 + 3H2SO4 = 2MnSO4 + 5О2 + K2SO4 + 8H2O Классификация ОВР: примерыРазличают следующие типы окислительно-восстановительных реакций: Примеры химических превращений, относящихся к различным типам ОВР: (NH4)2Cr2O7 = N2 + Cr2O3 + 4H2O 2NaNO3 = 2NaNO2 + O2 3Cu + 8HNO3 = 3Cu(NO3)2 + 2NO + 4H2O 2Al + Fe2O3 = Al2O3 + 2Fe 3Br2 + 6KOH = 5KBr + KBrO3 + 6H2O 3HNO2 = HNO3 + 2NO + H2O 2NO2 + H2O = HNO3 + HNO2 4KClO3 = KCl + 3KClO4 2H2S + SO2 = 3S + 2H2O HOCl + HCl = H2O + Cl2 Токовые и бестоковые ОВР
Первый случай — это получение электрической энергии за счёт химической реакции (такие источники энергии могут использоваться в двигателях машин, в радиотехнических устройствах, приборах управления), либо электролиз, то есть химическая реакция, наоборот, возникает за счёт электроэнергии (с помощью электролиза можно получать различные вещества, обрабатывать поверхности металлов и изделий из них). Примерами бестоковых ОВР можно назвать процессы горения, коррозии металлов, дыхания и фотосинтеза и т.д. Метод электронного баланса ОВР в химии
Основывается метод на том, что сумма принимаемых окислителем электронов и количество отдаваемых восстановителем приводится к равновесию. Метод складывается из нескольких этапов: На простом примере взаимодействия алюминия с кислородом удобно написать уравнивание поэтапно: 4Al + 3O2 = Al2O3 4Al + 3O2 = 2Al2O3 Примеры заданий на составление электронного балансаМогут встречаться следующие задания на уравнивания ОВР:
KCl + KMnO4 + H2SO4 = Cl2 + MnSO4 + K2SO4 + H2O Как видно после расстановки СО, атомы хлора отдают электроны, повышая свою СО до 0, а атомы марганца электроны принимают: Mn +7 +5е = Mn +2 множитель два; Проставляем в уравнение коэффициенты в соответствии с подобранными множителями: Уравниваем количество остальных элементов: 10KCl + 2KMnO4 + 8H2SO4 = 5Cl2 + 2MnSO4 + 6K2SO4 + 8H2O Cu + HNO3(конц.) = NO2 + Cu(NO3)2 + 2H2O Как видно, атомы меди повышают свою СО с нуля до двух, а атомы азота — снижают с +5 до +4 N +5 +1е = N +4 множитель два. Проставляем в уравнение коэффициенты: Уравниваем остальные элементы: Cu + 4HNO3(конц.) = 2NO2 + Cu (NO3)2 + 2H2O Запишем схему реакции, расставим СО: 2Cr +6 +6e = 2Cr +3 коэффициент 1. К2Сr2О7 + 3Н2S + Н2SО4 = 3S + Сr2(SО4)3 + K2SO4 + Н2О Уравниваем остальные элементы: К2Сr2О7 + 3Н2S +4Н2SО4 = 3S + Сr2(SО4)3 + K2SO4 + 7Н2О Влияние реакционной средыХарактер среды влияет на протекание тех или иных ОВР. Роль реакционной среды можно проследить на примере взаимодействия перманганата калия (KMnO4) и сульфита натрия (Na2SO3) при различных значениях рН: Видно, что изменение кислотности среды приводит к образованию разных продуктов взаимодействия одних и тех же веществ. При изменении кислотности среды они происходят и для других реагентов, вступающих в ОВР. Аналогично показанным выше примерам реакции с участием дихромат-иона Cr2O7 2- будут проходить с образованием разных продуктов реакции в различных средах: в кислой среде продуктом будет Cr 3+ ; в нейтральной — Cr2O3. Окислительно-восстановительные реакции (ОВР)Все химические реакции можно разделить на два типа: 1) Реакции, которые протекают без изменения степеней окисления элементов: степени окисления всех элементов в молекулах исходных веществ равны степеням окисления этих элементов в молекулах продуктов реакции. Например: 2) Реакции, которые протекают с изменением степеней окисления элементов: степени окисления всех или некоторых элементов в молекулах исходных веществ не равны степеням окисления этих элементов в молекулах продуктов реакции. Например: Реакции второго типа называются окислительно-восстановительными. Окислительно-восстановительные реакции (ОВР) — это химические реакции, при протекании которых степени окисления элементов изменяются. Изменение степеней окисления в ходе ОВР обусловлено полным или частичным переходом электронов от атомов одного элемента к атомам элемента. Так, в реакции 4.1.2 каждый атом магния отдает 2 электрона: Mg 0 = Mg +2 + 2ē (или: Mg 0 — 2ē = Mg +2 ) (4.1.4) Эти электроны переходят к молекуле кислорода. Каждый атом кислорода в молекуле О2 присоединяет 2 электрона, поэтому молекула кислорода присоединяет 4 электрона: Атом марганца, который в исходном веществе (KМnО4) имеет степень окисления +7, присоединяет 5 электронов и превращается в атом марганца со степенью окисления +2 (такую степень окисления он имеет в молекуле продукта реакции MnCl2): Mn +7 + 5ē = Mn +2 (4.1.7) Рассмотренный выше механизм ОВР объясняет, почему эти реакции называют реакциями с переносом электронов. Реакции, при протекании которых степени окисления не изменяются, называются реакциями без переноса электронов. Таким образом, любая ОВР представляет собой совокупность процессов отдачи и присоединения электронов. Процесс отдачи электронов называется окислением. В результате процесса окисления алгебраическая величи на степени окисления элемента повышается. В рассмотренных примерах процессы 4.1.4 и 4.1.6 являются процессами окисления. Процесс присоединения электронов называется восстановлением. В результате процесса восстановления алгебраическая величина степени окисления понижается. Процессы 4.1.5 и 4.1.7 являются примерами процессов восстановления. Частицы (атомы, молекулы, ионы), которые отдают электроны, называются восстановителями. В реакциях 4.1.2 и 4.1.3 восстановителями являются соответственно Mg и НCl. Частицы, которые присоединяют электроны, называются окислителями. В реакциях 4.1.2 и 4.1.3 окислителями являются соответственно O2 и KМnО4. Следовательно, в общем виде окислительно-восстановительную реакцию можно представить следующей схемой: Восстановитель + Окислитель = Продукты реакции Восстановитель участвует в процессе окисления, т. е. окисляется. А окислитель участвует в процессе восстановления, т. е. восстанавливается. Важнейшие окислители и восстановители Какие же вещества могут быть окислителями и какие восстановителями? Это зависит от величины степеней окисления элементов, которые входят в состав данных веществ. Как известно, некоторые элементы имеют постоянные степени окисления во всех или в большинстве сложных веществ. Для таких элементов изменение степеней окисления нехарактерно. Поэтому свойства веществ обычно не зависят от присутствия этих элементов. Элементы с переменной степенью окисления, как правило, легко ее изменяют, т. е. могут участвовать в процессах отдачи или присоединения электронов. Поэтому свойства сложных веществ обусловлены наличием в их составе элементов с переменной степенью окисления. Если в состав вещества входит элемент с высшей степенью окисления, он может только понижать ее, т. е. участвовать в процессе восстановления. Следовательно, данное вещество может только присоединять электроны и выступать только в роли окислителя. Например, свойства перманганата калия KМnО4 определяются степенью окисления марганца (калий и кислород — элементы с постоянной степенью окисления). Марганец в KМnО4 имеет высшую степень окисления +7, поэтому KМnО4 может быть только окислителем. Если в состав вещества входит элемент с низшей степенью окисления, он может только повышать ее, т. е. участвовать в процессе окисления. Следовательно, данное вещество может только отдавать электроны и выступать только в роли восстановителя. Например, свойства аммиака NH3 определяются степенью окисления азота (для водорода степень окисления +1 является практически постоянной). Азот в NH3 имеет низшую степень окисления —3, поэтому NH3 может быть только восстановителем. Если в состав вещества входит элемент с промежуточной степенью окисления, он может как повышать, так и понижать ее, т. е. может участвовать и в процессе окисления, и в процессе восстановления. Следовательно, данное вещество может быть и окислителем, и восстановителем. Это зависит от второго участника реакции. Например, свойства сульфита натрия Na2SО3 определяются степенью окисления серы, которая имеет промежуточную степень окисления +4. Поэтому Na2SО3 проявляет окислительно-восстановительную двойственность. В реакции с перманганатом калия: сульфит натрия окисляется до сульфата натрия, т. е. выступает в роли восстановителя. Это обусловлено тем, что KМnО4 может быть только окислителем (см. выше). А в реакции с сероводородом: сульфит натрия восстанавливается до свободной серы, т. е. выступает в роли окислителя, так как H2S может быть только восстановителем (сера в H2S находится в низшей степени окисления). Важнейшими окислителями являются: б) сложные вещества, молекулы которых содержат элементы в высшей степени окисления — перманганат калия KМnО4, хроматы и дихроматы (например, дихромат калия K2СrО7), азотная кислота HNO3 и ее соли — нитраты, концентрированная серная кислота H2SO4, оксид свинца (IV) РbО2, хлорная кислота HClO4 и ее соли — перхлорат и др. Важнейшими восстановителями являются: Среди веществ, содержащих элементы в промежуточных степенях окисления, есть вещества, для которых более характерными являются или окислительные, или восстановительные свойства. Обычно являются окислителями галогены Сl2 и Br2, хлорноватистая кислота НClО и ее соли — гипохлориты, хлораты (KСlO3 и др.), оксид марганца (IV) МnO2, соли трехвалентного железа (FeCl3 и др.). Как правило, в роли восстановителей выступают водород Н2, углерод С, оксид углерода (II) СО, сульфиты металлов (Na2SO3 и др.), соли двухвалентного железа (FeSO4 и др.). Типы окислительно-восстановительных реакций Различают 3 типа окислительно-восстановительных реакций. 1) Межмолекулярные окислительно-восстановительные реакции. В этих реакциях элемент-окислитель и элемент-восстановитель входят в состав молекул различных веществ. Примерами данного типа реакций являются 2) Внутримолекулярные окислительно-восстановительные реакции. В этих реакциях элемент-окислитель и элемент-восстановитель входят в состав одного вещества. Например: К этому типу ОВР относятся многие реакции термического разложения веществ. З) Реакции самоокисления-самовосстановления, называемые также реакциями диспропорционирования. Это ОВР, при протекании которых один и тот же элемент, находящийся в промежуточной степени окисления, и окисляется и восстанавливается. Часть атомов данного элемента отдает электроны другой части атомов этого же элемента. Например: Составление уравнений окислительно-восстановительных реакций Для составления уравнений окислительно-восстановительных реакций часто используется специальный метод — метод электронного баланса. В основе его лежит следующее правило: общее число электронов, которые отдает восстановитель, должно быть равно общему числу электронов, которые присоединяет окислитель. Рассмотрим применение метода электронного баланса на примере реакции, которая выражается следующей схемой: а) Определим степени окисления всех элементов в молекулах исходных веществ и продуктов реакции: б) Подчеркнем символы элементов, которые изменяют степени окисления в ходе реакции: в) Составим уравнения процессов окисления и восстановления: Обратите внимание, что в левой части уравнения процесса окисления взято два атома брома, так как продуктом окисления является двухатомная молекула брома Br2. г) Находим множители для уравнений процессов окисления и восстановления, при умножении на которые числа отданных и присоединенных электронов будут равны. Так как наименьшим общим кратным чисел «5» и «2» является «10», то уравнение процесса восстановления нужно умножить на «2», а уравнение процесса окисления — на «5»: д) Найденные множители запишем как коэффициенты перед формулами веществ, которые содержат элементы, участвующие в процессах окисления и восстановления: е) После этого уравниваем числа атомов элементов, которые не изменяют степени окисления. В данном случае это атомы калия, серы, водорода и кислорода. Обычно числа атомов водорода и кислорода уравнивают в последнюю очередь. Во многих случаях равенство чисел атомов кислорода в левой и в правой частях уравнения ОВР свидетельствует о том, что это уравнение составлено правильно (в составленном уравнении 40 атомов кислорода и в левой, и в правой частях). Рассмотрим некоторые более сложные примеры составления уравнений ОВР. Составим уравнение реакции, которая протекает по следующей схеме: Определим степени окисления всех элементов и подчеркнем символы элементов, которые изменяют свои степени окисления: Составим уравнения процессов окисления и восстановления и найдем множители, на которые нужно умножить эти уравнения: Обратите внимание, что не все атомы азота, которые входят в состав HNО3, изменяют свою степень окисления: часть атомов азота без изменения степени окисления переходит в молекулы Cu(NO3)2 Поэтому найденные методом электронного баланса коэффициенты напишем перед всеми формулами, содержащими Сu и N, кроме формулы HNO3: Коэффициент перед формулой HNO3 равен общему числу атомов азота в правой части уравнения, т. е. равен 8 (из них 6 атомов, которые не изменяют степень окисления): В последнюю очередь уравниваем числа атомов водорода и кислорода: В некоторых ОВР более двух элементов изменяют свои степени окисления. В качестве примера рассмотрим следующую реакцию: Два элемента — фосфор и сера — в ходе этой реакции окисляются, один элемент — азот — восстанавливается: Общее число электронов, которые участвуют в процессах окисления, равно 22; в процессе восстановления участвует 1 электрон. Поэтому общий множитель для двух уравнений процессов окисления равен 1, а множитель для уравнения процесса восстановления равен 22. Запишем эти множители в качестве коэффициентов перед формулами соответствующих веществ: В заключение уравняем числа атомов водорода и кислорода: |

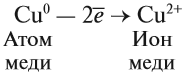

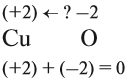
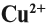
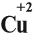
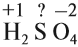
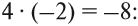
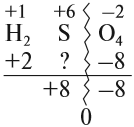
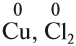
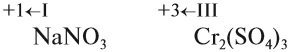
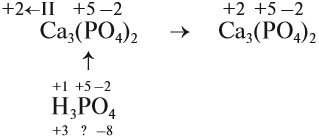
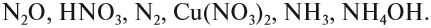
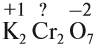
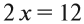
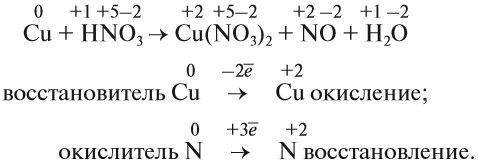
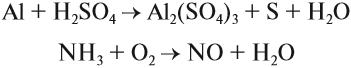
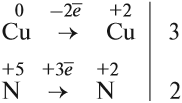
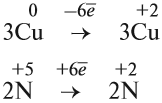
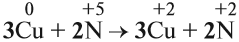
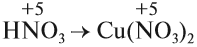
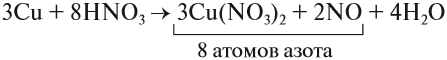
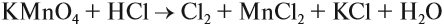
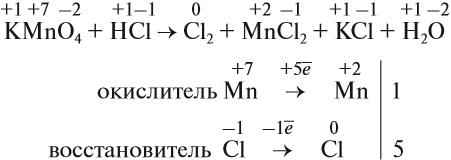
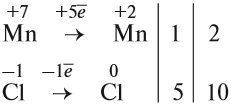
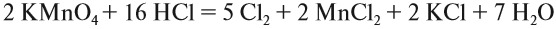
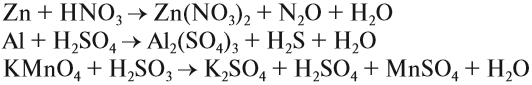

 На основе периодического закона химических элементов чаще всего можно предположить окислительно-восстановительные способности атомов того или иного элемента. По уравнению реакции также несложно понять, какие из атомов являются окислителем и восстановителем.
На основе периодического закона химических элементов чаще всего можно предположить окислительно-восстановительные способности атомов того или иного элемента. По уравнению реакции также несложно понять, какие из атомов являются окислителем и восстановителем. Атомы, имеющие промежуточные СО, способны и принимать и отдавать электроны, в результате этого вещества, содержащие в своём составе такие атомы, будут иметь возможность проявить себя как окислителем, так и восстановителем.
Атомы, имеющие промежуточные СО, способны и принимать и отдавать электроны, в результате этого вещества, содержащие в своём составе такие атомы, будут иметь возможность проявить себя как окислителем, так и восстановителем. Окислительно-восстановительные реакции также разделяют на токовые и бестоковые.
Окислительно-восстановительные реакции также разделяют на токовые и бестоковые. Уравнения большинства химических реакций уравниваются несложным подбором стехиометрических коэффициентов. Однако при подборе коэффициентов для ОВР можно столкнуться с ситуацией, когда количество атомов одних элементов не удаётся уравнять, не нарушая при этом равенство количеств атомов других. В уравнениях таких реакций подбирают коэффициенты методом составления электронного баланса.
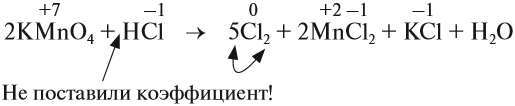
Уравнения большинства химических реакций уравниваются несложным подбором стехиометрических коэффициентов. Однако при подборе коэффициентов для ОВР можно столкнуться с ситуацией, когда количество атомов одних элементов не удаётся уравнять, не нарушая при этом равенство количеств атомов других. В уравнениях таких реакций подбирают коэффициенты методом составления электронного баланса.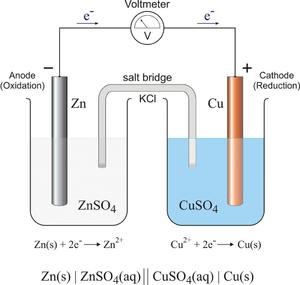 Марганцевокислый калий KMnO4 (перманганат калия, «марганцовка») — сильный окислитель за счёт того, что в KMnO4 степень окисления Mn равна +7. С его помощью часто получают газообразный хлор в лабораторных условиях по следующей реакции:
Марганцевокислый калий KMnO4 (перманганат калия, «марганцовка») — сильный окислитель за счёт того, что в KMnO4 степень окисления Mn равна +7. С его помощью часто получают газообразный хлор в лабораторных условиях по следующей реакции:


























