Сколько смеси в 1 куб м раствора
В нашей повседневной рабочей деятельности мы очень часто сталкиваемся с вопросами конвертации одних единиц измерения в другие. Зачастую перевести одну единицу измерения в другую не составляет труда, используя табличные значения нормативных документов (ГОСТ, СНИП и проч), а иногда, принципы конвертации неочевидны и требуют дополнительных расчетов. В этой статье мы хотим поделиться с вами нашим опытом в решении задачи о том, как связать между собой количество кубов раствора и количество сухой смеси в килограммах. Мы не будем рассматривать все возможные комбинации, а представим принцип решения на конкретном примере, разобравшись в котором вы без проблем сможете решить любую аналогичную задачу. Ведь хорошо известно, что поняв один принцип, не нужно помнить тысячу вещей. Итак, поехали!
В этой статье мы ответим на три вопроса, связанных между собой:
Введение
В вопросе №1 мы выясним, сколько потребуется мешков смеси для получения 1 кубического метра готового раствора. Мы знаем, что раствор это сочетание «вода + смесь» в определенной пропорции. Мы берем некий объем смеси, добавляем некий объем воды (согласно инструкции) и получаем определенный объем раствора.
Важно помнить, что полученный объем раствора часто совсем не равен объему конечного результата, например, из 1м3 раствора пескобетона мы не получим 1м3 готовой стяжки (вода испаряется, смесь дает усадку). Мы выясним, по сути, какую усадку дает готовый раствор при высыхании. Как это сделать рассмотрим в ответе на вопрос №2.
Вопрос №3 тесно связан с вопросами №1 и №2, и, чтобы на него ответить, нужно решить первые две задачи. Вам, возможно, также будет интересна наша статья на gipsoplita.ru, где мы описали способ расчета расхода стяжки под уклоном.
1. Сколько сухой смеси в 1 м3 готового раствора
Чтобы получить 1 куб. метр готового раствора сколько потребуется сухой смеси? Это самый непростой и самый частый вопрос, который возникает у потребителей. Однако, вся сложность вопроса заключается исключительно в доступности информации. Перейдем к деталям.
Источником информации для расчета будет (и должен) являться только официальный сайт производителя выбранной вами смеси. И вам очень повезло, если производитель указал в описании выход готового раствора, тогда ничего считать не придется. Если такой информации на сайте нет, то нужно считать вручную.
Итак, для расчета нам потребуются две характеристики:
Выглядеть это будет примерно так (см рисунок 1):
Для примера мы взяли пескобетон фирмы «Русеан».
Пример расчета. Исходя из указанных выше характеристик мы видим, что 1 м3 раствора весит 2000 кг (2 тонны). Чтобы получить раствор, мы должны замешать воду и смесь из расчета 0,13 литров на 1 кг смеси. Если считать, что 1 литр воды весит 1 кг, то раствор полученный из 1 кг смеси будет весить 1 кг + 0,13 кг = 1,13 кг.
Далее, мы помним, что 1 куб. метр раствора весит 2000 кг. Следовательно нам необходимо выяснить, сколько таких частей по 1,13 кг поместиться в 2000 кг, для этого просто делим 2000/1,13 кг = получаем число 1770.
Это число означает, что нам нужно взять ( 1 кг смеси + 0,13 л воды) и сложить их 1770 раз и тогда мы получим 1 кубический метр раствора, весом 2000 кг.
Итак ответ, для 1 м3 раствора пескобетона потребуется 1770 кг сухой смеси.
[ Вес 1м3 раствора ] / [(1 кг смеси + вес количества воды)]
Сложность, о которой мы говорили в начале главы, заключается в том, что далеко не каждый производитель указывает у себя на сайте «плотность раствора», поэтому придется самостоятельно запрашивать этот показатель напрямую у производителя или через выбранного вами дистрибьютора.
2. Сколько сухой смеси в 1 м3 стяжки
Дать ответ на этот вопрос проще всего рассмотрев конкретный пример расчета. Допустим, перед нами стоит задача сделать стяжку пола объемом 1 куб. Вопрос, сколько потребуется сухой смеси для решения поставленной задачи?
Первое, и единственное, с чего следует начать, это выяснить расход сухой смеси. Эту характеристику любой производитель обязан указывать и на упаковке, и на официальном сайте. Вот как это должно выглядеть (см рисунок 3)
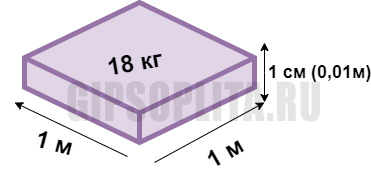
На рисунке мы видим расход при толщине слоя 10 мм (1 см). Это означает, что на основание со сторонами 1м и 1м (1м * 1м = 1 м2), и толщиной слоя 1 см (0,01м) у нас уйдет 18 кг смеси. Изобразим это на схеме (см рисунок 4)
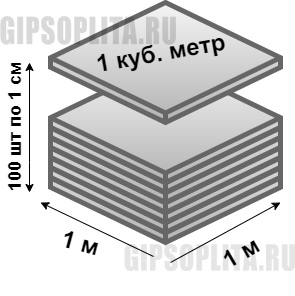
Мы получили такой кусок (срез) толщиной 1 см. Теперь, вопрос, а что такое 1 м3? Это ни что иное, как пачка (стопка) из 100 шт таких кусков по 1 см. Один кубический метр, это куб в основании которого квадрат со сторонами 1 метр на 1 метр, и высотой 1 метр (1м * 1м * 1м = 1 м3). А поскольку в метре 100 сантиметров, нужно взять 100 таких кусков толщиной 1 см и получим 1 кубический метр (см рисунок 5)
Далее все просто, мы знаем, что на 1 элемент уходит 18 кг смеси, то на 100 элементов уйдет 18*100 = 1800 кг смеси. Это и есть ответ.
Итак, обернем все в формулу:
РАСХОД (кг/м2 при слое 1 см) * 100 * КОЛ-ВО КУБОВ = КОЛ-ВО СМЕСИ (КГ)
Пример. Для 5,3 кубических метров стяжки потребуется: 18 кг/м2/1см * 100 * 5,3 = 9540 кг
Примечание. Если производитель указал расход в расчете на 1 мм, то вместо 100, нужно умножать на 1000.
3. Сколько раствора для 1 м3 стяжки
Для решения этого вопроса, как и в разделе 2 мы будем использовать конкретный пример. Итак, снова задача: «Сколько потребуется кубов раствора пескобетона, чтобы сделать 1 м3 готовой стяжки». Вопрос кажется слегка запутанным, но есть хорошая новость, мы уже умеем это делать и делали это раньше. Итак алгоритм (идем от обратного):
На вопрос №1 мы нашли решение в предыдущем разделе, ответ получился 1800 кг.
Заключение
В этой статье мы рассматривали расход на примере стяжки из пескобетона, ввиду того что это самый популярный вопрос. Однако, ничто нас не ограничивает применить те же самые правила и методики расчета для любой смеси, будь то «плиточный клей», «штукатурка», «наливной пол», «шпатлевка» или даже «ремонтный состав». Принципы одни и те же.
Концентрация растворов. Способы выражения концентрации растворов.
Концентрация раствора может выражаться как в безразмерных единицах (долях, процентах), так и в размерных величинах (массовых долях, молярности, титрах, мольных долях).
Способы выражения концентрации растворов.
1. Массовая доля (или процентная концентрация вещества) – это отношение массы растворенного вещества m к общей массе раствора. Для бинарного раствора, состоящего из растворённого вещества и растворителя:

ω – массовая доля растворенного вещества;
mв-ва – масса растворённого вещества;
Массовую долю выражают в долях от единицы или в процентах.
2. Молярная концентрация или молярность – это количество молей растворённого вещества в одном литре раствора V:

C – молярная концентрация растворённого вещества, моль/л (возможно также обозначение М, например, 0,2 М HCl);
n – количество растворенного вещества, моль;
V – объём раствора, л.
Раствор называют молярным или одномолярным, если в 1 литре раствора растворено 1 моль вещества, децимолярным – растворено 0,1 моля вещества, сантимолярным – растворено 0,01 моля вещества, миллимолярным – растворено 0,001 моля вещества.
3. Моляльная концентрация (моляльность) раствора С(x) показывает количество молей n растворенного вещества в 1 кг растворителя m:

С (x) – моляльность, моль/кг;
n – количество растворенного вещества, моль;
4. Титр – содержание вещества в граммах в 1 мл раствора:

T – титр растворённого вещества, г/мл;
mв-ва – масса растворенного вещества, г;
5. Мольная доля растворённого вещества – безразмерная величина, равная отношению количества растворенного вещества n к общему количеству веществ в растворе:

N – мольная доля растворённого вещества;
n – количество растворённого вещества, моль;
nр-ля – количество вещества растворителя, моль.
Сумма мольных долей должна равняться 1:
Иногда при решении задач необходимо переходить от одних единиц выражения к другим:
М(Х) – молярная масса растворенного вещества;
ρ= m/(1000V) – плотность раствора. 6. Нормальная концентрация растворов (нормальность или молярная концентрация эквивалента) – число грамм-эквивалентов данного вещества в одном литре раствора.
Грамм-эквивалент вещества – количество граммов вещества, численно равное его эквиваленту.
Эквивалент – это условная единица, равноценная одному иону водорода в кислотоно-основных реакциях или одному электрону в окислительно – восстановительных реакциях.
Для записи концентрации таких растворов используют сокращения н или N. Например, раствор, содержащий 0,1 моль-экв/л, называют децинормальным и записывают как 0,1 н.

СН – нормальная концентрация, моль-экв/л;
z – число эквивалентности;
Коэффициент растворимости – отношение массы вещества, образующего насыщенный раствор при конкретной температуре, к массе растворителя:
Как определить расход раствора на куб, на метр квдратный кладки
Как говорит народная пословица: «Семь раз отмерь, один раз отрежь». Этот метод не устареет никогда. Каждый строитель знает, что перед тем как приступать к той или иной работе, нужно все тщательно просчитать, изучить и составить план. Для чего это нужно? Одна из причин – узнать нужное количество расходуемого материала, подсчитать, во сколько это обойдется, и приобрести все что нужно. Если вы планируете строить дом, вас может интересовать вопрос, каков расход раствора на 1 м2 кладки кирпича? Ведь вам нужно заранее купить все составляющие для смеси, такие как песок, цемент и другие расходные материалы. Обратите внимание, что на качество готовой стены влияют такие факторы: качество материала и качество раствора. Если стену построить неправильно, то могут возникнуть мостики холода. Поэтому важно правильно приготовить раствор и нанести нужное его количество. Прочитав данную информацию, вы узнаете расход раствора на кладку кирпича.
Что влияет на расход
Раствор – связующее звено между кирпичами. Без него произвести возвести стену невозможно. Он должен быть качественным, правильно приготовленным и иметь подходящую консистенцию. Один из важных моментов, которые нужно учитывать при расчете – это его вид состава. Самыми распространенными являются 4 типа раствора:
Это самые популярные смеси, которые применяют в строительстве. Но, вы должны знать, что не только они влияют на расход. Немаловажный фактором является и сам кирпич. Его размер, формат, способность поглощать воду и наличие пустот напрямую определяют, сколько раствора будет в 1 м2 кладки кирпича. В целом, расход на 1 м2 составляет 0,2–0,25 м3. Все сводится к тому, что роль играет толщина стены, будь то в полкирпича, один, полтора или два. Чем больше толщина, тем больший расход. То же касается формы кирпича. К примеру, если он крупный, то расход снижается, если он с отверстиями, то расход значительно увеличивается. Как производится расчет раствора для кладки кирпича?
РАСХОД РАСТВОРА НА 1 М3
Чтобы узнать количество раствора на 1м3 кладки кирпича, рассмотрим такие данные. Рядовой кирпич имеет размеры 250×120×65. Существуют некие стандарты, которые показывают, сколько раствора нужно на 1 м3кладки кирпича:
Получается, что на 1 стандартный кирпич, приходится 0,0006305 м3 раствора. Если перевести это в литры, то на 1 м2 толщиной 12 см, припадает 75 литров готовой смеси, а когда толщина равна 1,5 кирпичам (380 мм), расход увеличивается до 115 литров.
Если говорить об утолщенных изделиях (модулированных), то при их размерах 250×120×88, расход следующий:
Исходя из этих данных, видно, как размер материала влияет на расход раствора, на куб кладки кирпича. Есть некая закономерность: чем больше площадь, тем меньше требуется состава. Зная эти данные, вы можете приготовить нужное количество смеси для кладки. Вам остается подсчитать общий метраж и умножить его на расход за 1 м3. Теперь вы подготовлены и можете закупать материал для работы. Ниже приведена таблица, которая поможет вам узнать расход цемента и добавок, для получения идеальной консистенции состава.
Как определить сколько мешков цемента покупать
Теперь, давайте выясним расход цемента на 1 м2 кладки кирпича. Для этого, вы должны сделать 3 шага:
Исходя из данных, приведенных выше, расход готовой смеси на 1 м3, при толщине стены в 51 см, составляет 0,240 м3. Узнать общее количество можно, умножив объем кладки на расход за 1 м3. Вот что должно выйти: 71,808 нужно умножить на 0,240. Используя калькулятор, получаем 17,233 м3. Это число указывает, сколько цементного раствора потребуется для работы. Из него требуется вычесть исключительно количество цемента.
Если выбранная пропорция составляет соотношение компонентов 1:3, то получается следующее: 17,233 требуется разделить на 4. Теперь вы знаете, сколько цемента вам необходимо для качественного раствора. Это число равно 4,308 м3. Остается пойти в магазин и купить столько мешков цемента, сколько потребуется. Но, цемент в кубометрах не продают. Материал расфасован в мешки по 25 или 50 кг, поэтому следует перевести наш показатель в килограммы. Чтобы сделать это, требуется знать плотность отвердителя. Как правило, в среднем этот показатель равен 1300 кг/м3. Производим вычисления: 4,308×1300 = 5600 кг. Теперь, 5600 кг делим на 50 (количество кг в одном мешке) и получаем расход в 112 мешков.
Вот и все, систему вы поняли, осталось только поменять числа, подставить свои и произвести необходимые вычисления. Все что требуется – калькулятор под рукой и готовые данные. Если все правильно сделать, то вы сможете значительно сэкономить свои средства и избежать того, что на складе останутся лишние материалы.
Вычисление объема раствора вещества, который потребуется для реакции
Задание 19.
Вычислите объем раствора с массовой долей калий гидроксида 44% и плотностью 1.46 г/мл, необходимого для растворения алюминия массой 8.1 г. Какой объем водорода (н.у) при этом выделится.
Решение:
Уравнение реакции имеет вид;
8,1г х г у л
2Al + 2KOH + 6H2O = 2K[Al(OH)4] + 3H2↑
(2 . 27) (2 . 56) (3 . 22,4) л
Находим массу КОН, потраченную на растворение алюминия из пропорции, получим:
8,1 г : х г = (2 . 27) : (2 . 56);
Находим массу раствора, получим:
Находим объем раствора КОН, получим:
V(KOH) = m(p-pa)/p(p-pa) = 38,18/1,46 = 26,15 мл.
Находим объем водорода, который выделится при реакции из пропорции, получим:
8,1г г : у л = (2 . 27) г : (3 . 22,4) л;
Ответ: V(KOH) = 26,15 мл; V(Н2) = 10,8 л.
Уравнение реакции имеет вид:
Из уравнения реакции следует, что 1 моль Ni(No3)2 реагирует с 2 моль NaOH.
Рассчитаем массу Ni(No3)2, потраченную на реакцию, получим:
Находим количество Ni(No3)2, получим:
n[Ni(No3)2] = m[Ni(No3)2]/M[Ni(No3)2] = 23,82/182,7 = 0,13 моль.
n(NaOH) = 2n[Ni(No3)2] = 2 . 0,13 = 0,26 моль.
Рассчитаем объем раствора NaOH, который потребуется для полного осаждения ионов никеля, получим:
Ответ: V(NaOH) = 2600 мл.
4.3.6. Расчеты массы (объема, количества вещества) продукта реакции, если одно из веществ дано в виде раствора с определенной массовой долей растворенного вещества.
Для расчета массы (объема, количества вещества) продукта реакции, если данные по одному из веществ представлены в виде раствора с определенной массовой долей этого растворенного вещества, следует воспользоваться нижеследующим алгоритмом:
1) Прежде всего следует найти массу растворенного вещества. Возможны две ситуации:
* В условии даны масса раствора и массовая доля растворенного вещества (концентрация). В этом случае масса растворенного вещества рассчитывается по формуле:
* В условии даны объем раствора вещества, плотность этого раствора и массовая доля растворенного вещества в этом растворе. В таком случае следует воспользоваться формулой для расчета массы раствора:
После чего следует рассчитать массу растворенного вещества по формуле 1.
2) Рассчитать количество вещества (моль) участника реакции, масса которого стала известна из расчетов выше. Для этого воспользоваться формулой:
3) Записать уравнение реакции и убедиться в правильности расставленных коэффициентов.
4) Рассчитать количество моль интересующего участника реакции исходя из известного количества другого участника реакции, зная, что количества веществ любых двух участников реакции A и B относятся друг к другу как коэффициенты перед этими же веществами в уравнении реакции, то есть:
Если в условии требовалось рассчитать количество вещества, то действия на этом заканчиваются. Если же требуется найти его массу или объем, следует переходить к следующему пункту.
5) Зная количество вещества, определенное в п.4, мы можем рассчитать его массу по формуле:
Также, если вещество является газообразным и речь идет о нормальных условиях (н.у.), его объем может быть рассчитан по формуле:
Рассмотрим пару примеров расчетных задач по этой теме.
Пример 1
Рассчитайте массу осадка, который образуется при добавлении к 147 г 20%-ного раствора серной кислоты избытка раствора нитрата бария.
Решение:
1) Рассчитаем массу чистой серной кислоты:
2) Рассчитаем количество вещества (моль) серной кислоты:
3) Запишем уравнение взаимодействия серной кислоты с нитратом бария:
4) В результате расчетов стало известно количество вещества серной кислоты. Осадок представляет собой сульфат бария. Зная, что:
n(BaSO4)/n(H2SO4) = k(BaSO4)/k(H2SO4), где n — количество вещества, а k — коэффициент в уравнении реакции,
5) Тогда масса осадка, т.е. сульфата бария, может быть рассчитана следующим образом:
m(BaSO4) = M(BaSO4) ∙ n(BaSO4) = 233 г/моль ∙ 0,3 моль = 69,9 г
Пример 2
Какой объем газа (н.у.) выделится при растворении необходимого количества сульфида железа (II) в 20%-ном растворе соляной кислоты с плотностью 1,1 г/мл и объемом 83 мл.
Решение:
1) Рассчитаем массу раствора соляной кислоты:
m(р-ра HCl) = V(р-ра HCl) ∙ ρ(р-ра HCl) = 83 мл ∙ 1,1 г/мл = 91,3 г
Далее рассчитаем массу чистого хлороводорода, входящего в состав кислоты:
m(HCl) = m(р-ра HCl) ∙ w(HCl)/100% = 91,3 г ∙ 20%/100% = 18,26 г
2) Рассчитаем количество вещества хлороводорода:
n(HCl) = m(HCl)/M(HCl) = 18,26 г/36,5 г/моль = 0,5 моль;
3) Запишем уравнение реакции сульфида железа (II) с соляной кислотой:
4) Исходя из уравнения реакции следует, что количество прореагировавшей соляной кислоты с количеством выделившегося сероводорода связано соотношением:
n(HCl)/n(H2S) = 2/1, где 2 и 1 — коэффициенты перед HCl и и H2S соответственно
n(H2S) = n(HCl)/2 = 0,5/2 = 0,25 моль
5) Объем любого газа, находящегося при нормальных условиях, можно рассчитать по формуле V(газа) = Vm ∙ n(газа), тогда:
V(H2S) = Vm ∙ n(H2S) = 22,4 л/моль ∙ 0,25 моль = 5,6 л