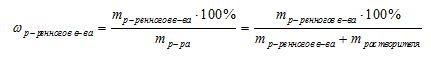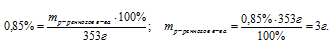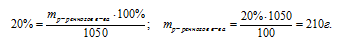Концентрация растворов. Способы выражения концентрации растворов.
Концентрация раствора может выражаться как в безразмерных единицах (долях, процентах), так и в размерных величинах (массовых долях, молярности, титрах, мольных долях).
Способы выражения концентрации растворов.
1. Массовая доля (или процентная концентрация вещества) – это отношение массы растворенного вещества m к общей массе раствора. Для бинарного раствора, состоящего из растворённого вещества и растворителя:

ω – массовая доля растворенного вещества;
mв-ва – масса растворённого вещества;
Массовую долю выражают в долях от единицы или в процентах.
2. Молярная концентрация или молярность – это количество молей растворённого вещества в одном литре раствора V:

C – молярная концентрация растворённого вещества, моль/л (возможно также обозначение М, например, 0,2 М HCl);
n – количество растворенного вещества, моль;
V – объём раствора, л.
Раствор называют молярным или одномолярным, если в 1 литре раствора растворено 1 моль вещества, децимолярным – растворено 0,1 моля вещества, сантимолярным – растворено 0,01 моля вещества, миллимолярным – растворено 0,001 моля вещества.
3. Моляльная концентрация (моляльность) раствора С(x) показывает количество молей n растворенного вещества в 1 кг растворителя m:

С (x) – моляльность, моль/кг;
n – количество растворенного вещества, моль;
4. Титр – содержание вещества в граммах в 1 мл раствора:

T – титр растворённого вещества, г/мл;
mв-ва – масса растворенного вещества, г;
5. Мольная доля растворённого вещества – безразмерная величина, равная отношению количества растворенного вещества n к общему количеству веществ в растворе:

N – мольная доля растворённого вещества;
n – количество растворённого вещества, моль;
nр-ля – количество вещества растворителя, моль.
Сумма мольных долей должна равняться 1:
Иногда при решении задач необходимо переходить от одних единиц выражения к другим:
М(Х) – молярная масса растворенного вещества;
ρ= m/(1000V) – плотность раствора. 6. Нормальная концентрация растворов (нормальность или молярная концентрация эквивалента) – число грамм-эквивалентов данного вещества в одном литре раствора.
Грамм-эквивалент вещества – количество граммов вещества, численно равное его эквиваленту.
Эквивалент – это условная единица, равноценная одному иону водорода в кислотоно-основных реакциях или одному электрону в окислительно – восстановительных реакциях.
Для записи концентрации таких растворов используют сокращения н или N. Например, раствор, содержащий 0,1 моль-экв/л, называют децинормальным и записывают как 0,1 н.

СН – нормальная концентрация, моль-экв/л;
z – число эквивалентности;
Коэффициент растворимости – отношение массы вещества, образующего насыщенный раствор при конкретной температуре, к массе растворителя:
Формула массы раствора
Определение и формула массы раствора
В лабораториях и промышленности чаще имеют дело не с индивидуальными веществами, а с гетерогенными или гомогенными смесями двух и более вещества. Гомогенные смеси веществ переменного состава называют растворами. Компонент раствора, концентрация которого выше других компонентов, является растворителем. Растворитель сохраняет свое фазовое состояние при образовании раствора. Различают газовые, жидкие и твердые растворы.
При вычислении концентрации какого-либо компонента жидкого раствора важно знать и уметь рассчитывать величину массы раствора. Это сумма масс всех компонентов, составляющих раствор (и растворенных веществ, и растворителя).
Для вычисления массы раствора можно использовать следующие формулы:
где msolute – масса растворенного вещества, а w — массовая концентрация (доля) растворенного вещества в растворе, выраженная в процентах;
где r — плотность раствора (г/см 3 ), а V – объем раствора.
Примеры решения задач
| Задание | Вычислите массу кремния, который может прореагировать с горячим раствором щелочи объемом 200 мл (массовая доля NaOH 35%, плотность 1,38 г/мл). Определите объем водорода, выделяющегося в результате этой реакции. |
| Решение | Рассчитаем массу раствора гидроксида натрия: |
msolution (NaOH) = V(NaOH) × ρ(NaOH);
msolution (NaOH) = 200× 1,38 = 276 г.
Тогда, масса гидроксида натрия будет равна:
msolute (NaOH)= 276 × 35/100% = 96,6 г.
Вычислим количество моль гидроксида натрия (молярная масса – 40 г/моль):
n(NaOH) = m(NaOH) / M(NaOH);
n(NaOH) = 96,6 / 40 = 2,415 моль.
Запишем уравнение реакции взаимодействия кремния с горячим раствором щелочи:
Согласно уравнению реакции n(NaOH) : n(Si) = 4:1, значит:
n(Si) = 0,25 × 2,415 = 0,6 моль.
Тогда, масса кремния (молярная масса – 28 г/моль) будет равна:
m(Si) = 0,6 × 28 = 16,8 г.
Для того, чтобы вычислить объем выделившегося водорода, рассчитаем его количество вещества. Согласно уравнению реакции n(NaOH) : n(H2) = 4:2, значит:
n(H2) = 0,5 × 2,415 = 1,25 моль.
Тогда, объем выделившегося водорода будет равен:
V(H2) = 1,25 × 22,4 = 28 л.
| Задание | Вычислите массу гидроксида калия, который требуется для приготовления раствора щелочи объемом 20 мл (массовая доля KOH 20%, плотность 1,22 г/мл). |
| Решение | Найдем массу раствора гидроксида калия: |
msolution = 20 × 1,22 = 24,4 г.
Тогда, масса гидроксида калия, который требуется для приготовления щелочи будет равна:
msolute (KOH) = ω (KOH) / 100% ×msolution;
msolute (KOH) = 20 / 100% × 24,4 = 4,48 г.
Копирование материалов с сайта возможно только с разрешения
администрации портала и при наличие активной ссылки на источник.
Вычисление массы/массовой доли вещества в растворе

ω(Х) = m(Х)/М(р-ра) (в долях единицы);
ω(Х) = m(Х)• 100/М(р-ра) (в процентах).
Молярной концентрацией называют количество растворенного вещества в 1 л раствора. Ее обозначают символом с(Х) и измеряют в моль/л:
В этой формуле n(Х) — количество вещества Х, содержащегося в растворе, M(X) — молярная масса вещества Х.
Рассмотрим несколько типовых задач.
Решение.
Массу бромида натрия определим по формуле: m(NaBr) = ω • М(р-ра)/100;
m(NaBr) = 15•300/100 = 45 г.
Ответ: 45 г.
2. Масса нитрата калия, которую нужно растворить в 200 г воды для получения 8%-ного раствора, равна ______ г. (Ответ округлите до целого числа.)
Решение.
Пусть m(KNO3) = x г, тогда М(р-ра) = (200 + х) г.
Массовая доля нитрата калия в растворе:
ω(KNO3) = х/(200 + х) = 0,08;
х = 16 + 0,08х;
0,92х = 16;
х = 17,4.
После округления х = 17 г.
Ответ: 17 г.
3. Масса хлорида кальция, которую нужно добавить к 400 г 5%-ного раствора этой же соли, чтобы удвоить ее массовую долю, равна______ г. (Ответ запишите с точностью до десятых.)
Решение.
Масса CaCl2 в исходном растворе равна:
m(CaCl2) = ω • М(р-ра);
m(CaCl2) = 0,05 • 400 = 20 г.
Массовая доля CaCl2 в конечном растворе равна ω 1 = 0,05 • 2 = 0,1.
Пусть масса CaCl2, которую нужно добавить в исходный раствор, равна х г.
Тогда масса конечного раствора М1(р-ра) = (400 + х) г.
Массовая доля CaCl2 в конечном растворе:
Решив это уравнение, получим х = 22,2 г.
Ответ: 22,2 г.
4. Масса спирта, которую нужно испарить из 120 г 2%-ного спиртового раствора йода, чтобы повысить его концентрацию до 5%, равна _____________ г. (Ответ запишите с точностью до десятых.)
Решение.
Определим массу йода в исходном растворе:
m(I2) = ω • М(р-ра);
m(I2) = 0,02•120 = 2,4 г,
После выпаривания масса раствора стала равна:
М1(р-ра) = m(I2)/ω 1
М1(р-ра) =2,4/0,05 = 48 г.
По разности масс растворов находим массу испарившегося спирта: 120-48 = 72 г.
Ответ: 72 г.
5. Масса воды, которую нужно добавить к 200 г 20%-ного раствора бромида натрия, чтобы получить 5%-ный раствор, равна_________ г. (Ответ округлите до целого числа.)
Решение.
Определим массу бромида натрия в исходном растворе:
m(NaBr) = ω • М(р-ра);
m(NaBr) = 0,2 • 200 = 40 г.
Пусть масса воды, которую нужно добавить для разбавления раствора, равна x г, тогда по условию задачи:
Отсюда получим x = 600 г.
Ответ: 600 г.
6. Массовая доля сульфата натрия в растворе, полученном при смешении 200 г 5%-ного и 400 г 10%-ного растворов Na2SO4, равна _____________ %. (Ответ округлите до десятых.)
Решение.
Определим массу сульфата натрия в первом исходном растворе:
m1(Na2SO4) = 0,05 • 200 = 10 г.
Определим массу сульфата натрия во втором исходном растворе:
m2(Na2SO4) = 0,1 • 400 = 40 г.
Определим массу сульфата натрия в конечном растворе: m(Na2SO4) = 10 + 40 = 50 г.
Определим массу конечного раствора:М(р-ра) = 200 + 400 = 600 г.
Определим массовую долю Na2SO4 в конечном растворе: 50/600 = 8,3%
Ответ: 8,3%.
В дополнение к решению задач на растворы:
“Правилом креста” называют диагональную схему правила смешения для случаев с двумя растворами.
Слева на концах отрезков записывают исходные массовые доли растворов (обычно слева вверху-большая), на пересечении отрезков — заданная, а справа на их концах записываются разности между исходными и заданной массовыми долями. Получаемые массовые части показывают в каком отношении надо слить исходные растворы.
Например: Определите, сколько нужно взять растворов соли 60%-й и 10%-й концентраций для приготовления 300 г раствора 25%-й концентрации.
Нужно смешать 90 г 60% раствора и 210 г 10% раствора.
Алгоритм нахождения массы раствора
Алгоритм нахождения массы раствора.
1.Прочтите текст задачи.
2.Запишите кратко условие и требование задачи с помощью общепринятых обозначений.
3.Запишите формулу для расчета массы раствора по массе его компонентов:
m (р-ра)= m (в-ва)+ m ( H 2 O )
5.Полученные в шагах 3и4 формулы сведите в одно уравнение с одним неизвестным х
(масса растворенного вещества) и решите его
6.Вычислите массу раствора по формуле (см. шаги 3 и 4)
1.Рассчитайте массу раствора, содержащего 160г. воды, если массовая доля сульфата меди в нем составляет 0,2.
7.Ответ: масса раствора 200г.
Курс повышения квалификации
Дистанционное обучение как современный формат преподавания
Курс повышения квалификации
Современные педтехнологии в деятельности учителя
Курс повышения квалификации
Педагогическая деятельность в контексте профессионального стандарта педагога и ФГОС
Ищем педагогов в команду «Инфоурок»
Номер материала: ДБ-1473730
Не нашли то что искали?
Вам будут интересны эти курсы:
Оставьте свой комментарий
Авторизуйтесь, чтобы задавать вопросы.
Путин поручил не считать выплаты за классное руководство в средней зарплате
Время чтения: 1 минута
ВПР для школьников в 2022 году пройдут весной
Время чтения: 1 минута
Учителям предлагают 1,5 миллиона рублей за переезд в Златоуст
Время чтения: 1 минута
В России утвердили новый порядок формирования федерального перечня учебников
Время чтения: 1 минута
НИУ ВШЭ откроет первую в России магистратуру по управлению низкоуглеродным развитием
Время чтения: 2 минуты
Минпросвещения планирует выделить «Профессионалитет» в отдельный уровень образования
Время чтения: 2 минуты
Подарочные сертификаты
Ответственность за разрешение любых спорных моментов, касающихся самих материалов и их содержания, берут на себя пользователи, разместившие материал на сайте. Однако администрация сайта готова оказать всяческую поддержку в решении любых вопросов, связанных с работой и содержанием сайта. Если Вы заметили, что на данном сайте незаконно используются материалы, сообщите об этом администрации сайта через форму обратной связи.
Все материалы, размещенные на сайте, созданы авторами сайта либо размещены пользователями сайта и представлены на сайте исключительно для ознакомления. Авторские права на материалы принадлежат их законным авторам. Частичное или полное копирование материалов сайта без письменного разрешения администрации сайта запрещено! Мнение администрации может не совпадать с точкой зрения авторов.
Методы решения расчетных задач по химии, связанные с концентрацией растворов
Во всех задачах этой группы присутствуют расчеты, связанные с концентрацией растворов. Причем во всех тестах используется единственный способ выражения концентрации — массовая доля. Поэтому при решении практически всех задач В9 мы будем пользоваться соотношением для определения массовой доли:
Анализ всех задач, предлагавшихся для решения, за последние годы позволяет распределить их на четыре группы:
1. Определение массы растворенного вещества в определенной порции раствора при известной концентрации;
2. Приготовление раствора путем растворения определенного количества вещества в некотором объеме (массе) растворителя;
3. Изменение концентрации уже имеющегося раствора одним из следующих способов:
а) добавлением к раствору того же растворенного вещества;
б) добавлением к раствору растворителя;
в) смешиванием двух различных растворов одного и того же вещества;
г) выпариванием растворителя или растворенного вещества из раствора.
4. Использование химической реакции в процессе приготовления раствора.
В этой статье,рассмотрим задачи 1-й из вышеперечисленных четырех групп.
Определение массы растворенного вещества в растворе
Ответ: масса растворенного вещества равна 3г.
Ответ: m(НNO3) 210 г.
Источник:
ЕГЭ. Химия. Расчетные задачи в тестах ЕГЭ. Части А, В, С / Д.Н. Турчен. — М.: Издательство «Экзамен», 2009. — 399 [1]с. (Серия «ЕГЭ. 100 баллов»). I8ВN 978-5-377-02482-8.