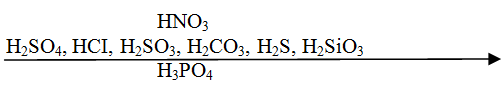Кислоты, их классификация
Урок 38. Химия 8 класс
В данный момент вы не можете посмотреть или раздать видеоурок ученикам
Чтобы получить доступ к этому и другим видеоурокам комплекта, вам нужно добавить его в личный кабинет, приобрев в каталоге.
Получите невероятные возможности
Конспект урока «Кислоты, их классификация»
Существует несколько признаков классификации кислот. Разберем некоторые их них. Кислоты – это сложные вещества, состоящие из атомов водорода и кислотных остатков.
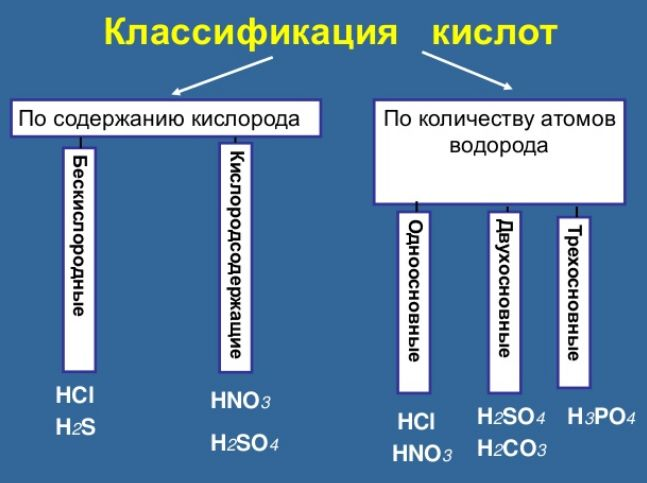
По наличию атомов кислорода в кислотах, кислоты делятся на кислородсодержащие, в которых присутствует кислород, например, серная кислота, азотная кислоты, бескислородные, в которых кислорода нет, к таким кислотам относится соляная, сероводородная.
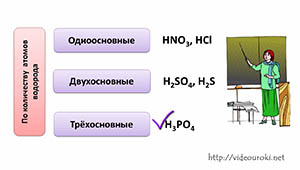
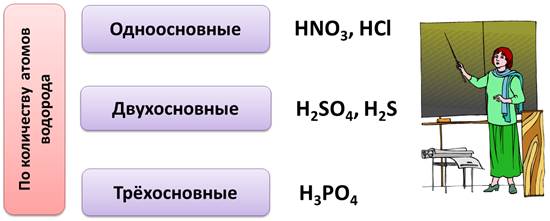
По количеству атомов водорода в кислоте, кислоты делятся на однооснòвные, у которых один атом водорода (например, в азотной кислоте, соляной), двухоснòвные, у которых 2 атома водорода (как в серной кислоте или сероводородной), трёхоснòвные, у которых 3 атома водорода (как в фосфорной кислоте).
По растворимости в воде кислоты делятся на растворимые в воде, к ним относится большинство кислот и нерастворимые в воде, как кремниевая кислота.
По летучести, т.е. способности молекул кислоты легко переходить в газообразное состояние, кислоты делятся на летучие (как соляная, сероводородная и азотная кислоты) и нелетучие – это большинство кислот: серная, кремниевая, фосфорная.
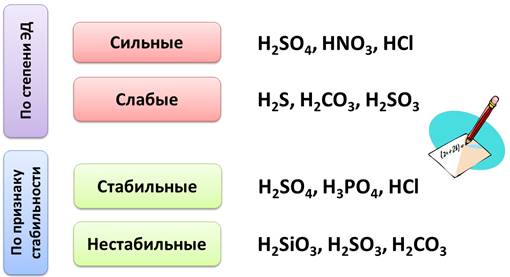
По степени электролитической диссоциации кислоты делятся на сильные, у которых степень электролитической диссоциации стремится к единице, к ним относятся такие кислоты, как серная, азотная, соляная, а слабые кислоты, у которых степень электролитической диссоциации стремится к нулю, например, сероводородная, угольная, сернистая.
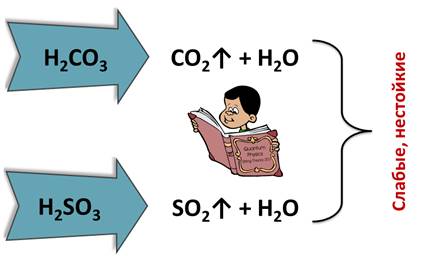
По признаку стабильности кислоты делят на стабильные, как серная, фосфорная, соляная, и нестабильные, которые разлагаются при обычных условиях или при нагревании, это такие кислоты, как кремниевая, сернистая, угольная.
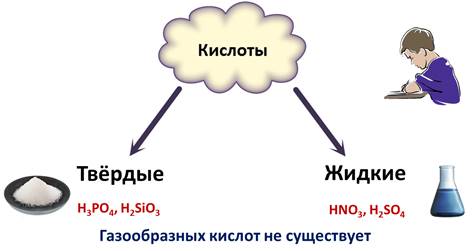
При обычных условиях кислоты могут быть твердыми. Это такие кислоты, как фосфорная и кремниевая. А также кислоты могут быть жидкими, как азотная, серная. Газообразных кислот при обычных условиях нет. Не путайте: соляную, сероводородную, бромоводородную кислоты образуют соответствующе газы, растворенные в воде, но они не являются газообразными кислотами.
Некоторые кислоты, такие как угольная и сернистая, существуют только в водных растворах, потому что они являются слабыми и нестойкими, они легко разлагаются на соответствующие оксиды и воду, поэтому выделить эти кислоты в чистом виде невозможно. Соляная кислота является летучей стабильной кислотой, а кремниевая кислота – нелетучей, нерастворимой и нестабильной кислотой, потому что при нагревании разлагается на оксид и воду.
Большинство водных растворов кислот не имеют окраски: серная, азотная, соляная и др., а хромовая (H2CrO4) имеет жёлтую окраску, марганцевая кислота (HMnO4) имеет малиновую окраску.
Виды кислот и способы их получения
В химии неорганические соединения делятся на простые и сложные вещества. Простые состоят из атомов одного химического элемента, сложные — из нескольких. Сложные неорганические вещества делятся на пять основных классов: кислоты, основания, амфотерные гидроксиды, оксиды, соли.
Разберёмся с первым классом из списка — кислотами.
Что такое кислота — определение в химии
Кислоты — это сложные вещества, которые состоят из атомов водорода и кислотных остатков.
A c — кислотный остаток;
x — число атомов водорода;
n — степень окисления кислотного остатка.
В химических реакциях активный атом водорода может замещаться на атом металла, в результате чего получается соль. Кислотный остаток — это часть молекулы кислоты без атомов водорода. Валентность кислотного остатка равна числу связанных с ним атомов водорода.
Виды кислот и их классификация, какие бывают (примеры)
Существуют несколько классификаций кислот. Разберёмся с основной классификацией, созданной по формальным признакам: содержанию кислорода, растворимости и так далее.
По содержанию кислорода
Кислоты могут делиться на кислородосодержащие и бескислородные.
Кислородсодержащие получаются при воздействии воды на кислотные оксиды — ангидриды.
Их название в корне содержит название элемента, входящего в состав ангидрида. Примеры:
Номенклатура выглядит следующим образом. В случае, если элементу соответствуют несколько кислот, для названия кислоты с большей валентностью такого элемента употребляют суффикс «Н» или «В». Для кислот с меньшей валентностью элемента в названиях добавляют еще один суффикс «ИСТ». Например, серная ( H 2 S O 4 ) и сернистая кислота ( H 2 S O 3 ).
Бескислородные представляют собой растворы некоторых газов в воде. Названия бескислородных кислот составляют по принципу: элемент + водородная кислота.
Важно, что газ и раствор газа имеют различные свойства. Например, хлороводород и соляная кислота.
Газ хлороводород можно получить из водорода и хлора. Уравнение:
H 2 + C l 2 → 2 H C l
В сухом состоянии такой газ не проявляет кислотных свойств. При перевозке в тех же металлических ёмкостях не происходит никаких реакций. Но, если хлороводород растворить в воде, получается раствор, который называют соляной кислотой. Она обладает сильными кислотными свойствами и опасна при реагировании с металлом.
По растворимости в воде
Кислоты делят на растворимые и нерастворимые. Большинство кислот растворимы. Нерастворимые — кремниевая H 2 S i O 3 и все органические карбоновые кислоты, содержащие десять атомов углерода и больше.
По летучести
Летучие кислоты — это химические соединения, которые быстро испаряются при нормальных условиях, то есть молекулы легко переходят в газовую фазу. В их список входят, к примеру, органические соединения, которые образуются в человеческом организме в результате процесса пищеварения, болезней или метаболизма.
Список летучих кислот:
Нелетучими являются все остальные. Они стабильны в водных растворах.
По силе (степени диссоциации)
Кислоты также можно разделить на сильные и слабые. Если в водном растворе кислота полностью распадается на ионы (диссоциирует), то она является сильной. Слабые кислоты не распадаются на ионы полностью, обычно их диссоциация протекает в незначительной степени.
Как определить силу кислоты, то есть степень диссоциации? Можно использовать лёгкий приём: вычесть из числа атомов O число атомов H. Если в ответе получается число меньше 2 — слабая. Больше или равно — сильная.
Степень диссициации можно также установить экспериментальным путем посредством измерения проводимости растворов. Разбавленные растворы сильных кислот хорошо проводят электрический ток, растворы слабых кислот — плохо.
Характерные химические и физические свойства
Химические свойства
Взаимодействие с основными оксидами. Образуются соль и вода:
C a O + 2 H C l → C a C l 2 + H 2 O
Взаимодействие с амфотерными оксидами. Образуются соль и вода:
Z n O + 2 H N O 3 → Z n ( N O 3 ) 2 + H 2 O
Взаимодействие со щелочами. Образуются соль и вода (реакция нейтрализации):
N a O H + H C l → N a C l + H 2 O
Взаимодействие с солями. Реакция протекает, если выпадает осадок или выделяется газ:
B a C l 2 + H 2 S O 4 → B a S O 4 ↓ + H C l ↑
Сильные кислоты вытесняют более слабые из их солей:
K 3 P O 4 + 3 H C l → 3 K C l + H 3 P O 4
Также металлы, стоящие в ряду активности до водорода, вытесняют его из раствора кислоты (если соль, которая образуется в итоге, растворима):
M g + 2 H C l → M g C l 2 + H 2 ↑
Однако! С азотной и концентрированной серной кислотами реакция идёт иначе:
M g + 2 H 2 S O 4 → M g S O 4 + S O 2 ↑ + 2 H 2
Физические свойства
Получение и применение кислот
Кислоты можно получить несколькими методами.
Взаимодействие кислотного оксида с водой:
H 2 O + S O 3 → H 2 S O 4
Взаимодействие водорода и неметалла:
H 2 + C l 2 → 2 H C l
Вытеснение слабой кислоты из солей более сильной кислотой:
3 H 2 S O 4 + 2 K 3 P O 4 → 3 K 2 S O 4 + H 3 P O 4
Кислоты находят широкое применение в различных сферах. К примеру, серная используется для производства лакокрасочных материалов и минеральных удобрений. Борная является медицинским антисептиком. Уксусную и лимонную добавляют при приготовлении выпечки, а аскорбиновую применяют при лечении простудных заболеваний.
Кислота
Кисло́ты — сложные вещества, в состав которых обычно входят атомы водорода, способные замещаться на атомы металлов, и кислотный остаток. Водные растворы кислот имеют кислый вкус, обладают раздражающим действием, способны менять окраску индикаторов, отличаются рядом общих химических свойств.
Содержание
Определение кислоты
Определения кислот и оснований претерпели значительную эволюцию по мере расширения теоретических представлений о природе химической связи и механизмах химических реакций.
В 1778 французский химик Антуан Лавуазье предположил, что кислотные свойства обусловлены наличием в молекуле атомов кислорода. Эта гипотеза быстро доказала свою несостоятельность, так как многие кислоты не имеют в своём составе кислорода, в то время как многие кислородсодержащие соединения не проявляют кислотных свойств. Тем не менее, именно эта гипотеза дала название кислороду как химическому элементу.
В 1839 немецкий химик Юстус Либих дал такое определение кислотам: кислота — это водородосодержащее соединение, водород которого может быть замещён на металл с образованием соли.
Первую попытку создать общую теорию кислот и оснований предпринял шведский физикохимик Сванте Аррениус. Согласно его теории, сформулированной в 1887, кислота — это соединение, диссоциирующее в водном растворе с образованием протонов (ионов водорода H + ). Теория Аррениуса быстро показала свою ограниченность, она не могла объяснить многих экспериментальных фактов. В наше время она имеет главным образом историческое и педагогическое значение.
В настоящее время наиболее распространены три теории кислоты и оснований. Они не противоречат друг другу, а дополняют.
Следует также отметить, что многие вещества проявляют амфотерные свойства, то есть ведут себя как кислоты в реакциях с основаниями и как основания — в реакциях с более сильной кислотой.
Классификация кислот
Химические свойства кислот
(в данном случае образуется неустойчивая угольная кислота 
Некоторые распространённые кислоты
Неорганические (минеральные) кислоты
Кислоты, образованные серой
Органические кислоты
Интересные факты
Примечания
См. также
| H + | Li + | K + | Na + | NH4 + | Ba 2+ | Ca 2+ | Mg 2+ | Sr 2+ | Al 3+ | Cr 3+ | Fe 2+ | Fe 3+ | Ni 2+ | Co 2+ | Mn 2+ | Zn 2+ | Ag + | Hg 2+ | Hg2 2+ | Pb 2+ | Sn 2+ | Cu + | Cu 2+ | |
| OH − | P | P | P | — | P | М | Н | М | Н | Н | Н | — | Н | Н | Н | Н | Н | — | — | Н | Н | Н | Н | |
| F − | P | Н | P | P | Р | М | Н | Н | М | Р | Н | Н | Н | Р | Р | М | Р | Р | М | М | Н | Р | Н | Р |
| Cl − | P | P | P | P | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Н | Р | Н | М | — | Н | Р |
| Br − | P | P | P | P | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Н | М | Н | М | Р | H | Р |
| I − | P | P | P | P | Р | Р | Р | Р | Р | Р | ? | Р | — | Р | Р | Р | Р | Н | Н | Н | Н | М | Н | — |
| S 2− | P | P | P | P | — | Р | М | Н | Р | — | — | Н | — | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н |
| SO3 2− | P | P | P | P | Р | М | М | М | Н | ? | ? | М | ? | Н | Н | Н | М | Н | Н | Н | Н | ? | Н | ? |
| SO4 2− | P | P | P | P | Р | Н | М | Р | Н | Р | Р | Р | Р | Р | Р | Р | Р | М | — | Н | Н | Р | Р | Р |
| NO3 − | P | P | P | P | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | — | Р | — | Р | Р |
| NO2 − | P | P | P | P | Р | Р | Р | Р | Р | ? | ? | ? | ? | Р | М | ? | ? | М | ? | ? | ? | ? | ? | ? |
| PO4 3− | P | Н | P | P | — | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | ? | Н | Н | Н | Н |
| CO3 2− | М | Р | P | P | Р | Н | Н | Н | Н | — | — | Н | — | Н | Н | — | Н | Н | — | Н | — | — | ? | — |
| CH3COO − | P | Р | P | P | Р | Р | Р | Р | Р | — | Р | Р | — | Р | Р | Р | Р | Р | Р | М | Р | — | Р | Р |
| CN − | P | Р | P | P | Р | Р | Р | Р | Р | ? | Н | Н | — | Н | Н | Н | Н | Н | Р | Н | Р | — | — | Н |
| SiO3 2− | H | Н | P | P | ? | Н | Н | Н | Н | ? | ? | Н | ? | ? | ? | Н | Н | ? | ? | ? | Н | ? | ? | ? |
Полезное
Смотреть что такое «Кислота» в других словарях:
кислота — сущ., кол во синонимов: 171 • абсцизин (2) • агарицин (1) • адипил (1) • … Словарь синонимов
КиСЛОТа — 1 капля Альбом ремиксов СЛОТ Дата выпуска 2008 Записан … Википедия
кислота — сущ., ж., употр. сравн. часто Морфология: (нет) чего? кислоты, чему? кислоте, (вижу) что? кислоту, чем? кислотой, о чём? о кислоте; мн. что? кислоты, (нет) чего? кислот, чему? кислотам, (вижу) что? кислоты, чем? кислотами, о чём? о кислотах 1.… … Толковый словарь Дмитриева
КИСЛОТА — КИСЛОТА, кислоты, мн. кислоты, жен. 1. только ед. отвлеч. сущ. к кислый, что нибудь кислое (разг.). Я попробовал, чувствую: кислота какая то. 2. Химическое соединение, обладающее кислым вкусом и окрашивающее синий лакмус в красный цвет (хим.).… … Толковый словарь Ушакова
кислота — КИСЛОТА, ы, мн. оты, от, жен. Химическое соединение, содержащее водород, дающее при реакции с основаниями (в 8 знач.) соли и окрашивающее лакмусовую бумагу в красный цвет. Азотная, уксусная к. | прил. кислотный, ая, ое. К. краситель. К. дождь (с… … Толковый словарь Ожегова
КИСЛОТА 1 — КИСЛОТА 1, Шы, мн. оты, от, ж. Химическое соединение, содержащее водород, дающее при реакции с основаниями (в 8 знач.) соли и окрашивающее лакмусовую бумагу в красный цвет. Азотная, уксусная к. Толковый словарь Ожегова. С.И. Ожегов, Н.Ю. Шведова … Толковый словарь Ожегова
КИСЛОТА 2 — см. кислый 1. Толковый словарь Ожегова. С.И. Ожегов, Н.Ю. Шведова. 1949 1992 … Толковый словарь Ожегова
кислота — КИСЛОТА, ы, ж Химическое соединение, обычно кислого вкуса, содержащее водород, способный замещаться металлом при образовании соли. Кислота окрашивает лакмусовую бумагу в красный цвет … Толковый словарь русских существительных
КИСЛОТА — КИСЛОТА, химическое соединение, содержащее водород, который может быть замещен металлом или другим положительным ионом с образованием соли. Кислоты растворяются в воде с получением ионов водорода (Н+), то есть действуют как источник протонов;… … Научно-технический энциклопедический словарь
кислота́ — кислота, ы; мн. кислоты, кислот … Русское словесное ударение
Кислота — ж. 1. Химическое соединение, содержащее водород, способный замещаться металлом при образовании соли. 2. То, что своими свойствами цветом, запахом, едкостью и т.п. напоминает такое химическое соединение. Толковый словарь Ефремовой. Т. Ф. Ефремова … Современный толковый словарь русского языка Ефремовой
Краткий конспект подготовки к ЗНО по химии №10 Кислоты
Подготовка к ВНО. Химия.
Конспект 10. Кислоты
Общая характеристика кислот
| Название кислоты | Формула кислоты | Кислотный остаток | Название солей |
| Фтороводородная (плавиковая) |  |  | Фторид |
| Хлороводородная (соляная) |  |  | Хлорид |
| Бромоводородная |  |  | Бромид |
| Угольная |  | =  | Карбонат |
| Кремниевая |  | =  | Силикат |
| Азотная |  |  | Нитрат |
| Ортофосфорная |  |  | Ортофосфат |
| Серная | =  | Сульфат | |
| Сернистая |  | =  | Сульфит |
| Сероводородная |  | =  | Сульфид |
Одним из представителей органических кислот является уксусная кислота 
Слово «кислота» по значению связано со словом «кислый», так как имеют общий корень. Отсюда следует, что растворы всех кислот имеют кислый вкус.
Несмотря на это, не следует пробовать на вкус никакие растворы кислот, так как некоторые из них относятся к едким и ядовитым растворам.
Природные источники кислот.
В природе встречается много кислот: лимонная кислота в лимонах, яблочная кислота – в яблоках, щавелевая кислота – в листьях щавеля.
Муравьи защищаются от врагов, выбрасывая едкие капельки муравьиной кислоты. (Она же содержится в пчелином яде и жгучих волосках крапивы.)
При прокисании виноградного сока получается всем известная уксусная кислота (уксус), а при прокисании молока – молочная кислота, та же самая молочная кислота получается при квашении капусты.
Кислоты делят на несколько групп. К каждой группе принадлежат кислоты, сходные по определенным признакам.
1. Существуют бескислородные и кислородсодержащие кислоты. Название этих групп указывает на наличие или отсутствие в молекуле кислоты атомов кислорода.
2. Другой признак классификации кислот – количество атомов водорода в кислоте. Соответствующую характеристику кислоты называют основностью. Существуют одно-, двух-, трехосновные кислоты.
3. Приведем еще один признак классификации кислот, как электролитов по степени электролитической диссоциации. Кислота – это электролит, водный раствор которого содержит катионы водорода и анионы кислотного остатка. Если электролит диссоциирует практически нацело – это сильный электролит. Электролит, степень диссоциации которого мала, это слабый электролит.
Классификация по степени электролитической диссоциации.
| Признак классификации | ||
| Степень электролитической диссоциации | Сильные кислоты |  |
| Слабые кислоты |  |
Физические свойства кислот
Агрегатное состояние.
При обычных условиях кислоты могут быть твердыми веществами(ортофосфорная 


Такие газы как хлороводород 


Цвет.
Водные растворы соляной, азотной, серной, ортофосфорной и ряда других кислот не имеют окраски. Водные растворы хромовой кислоты 

Запах.
Некоторые кислоты имеют запах. Например, кислоты: 
Растворением в воде сероводорода получают сероводородную кислоту 
Растворимость, летучесть и стабильность некоторых кислот.
| Физические свойства | Группы кислот | Пример |
| Растворимость | Растворимые |  |
| Нерастворимые |  | |
| Летучесть | Летучие |  |
| Нелетучие |  | |
| Стабильность | Стабильные |  |
| Нестабильные |  |
Серная, соляная, уксусная кислоты могут вызывать сильные ожоги, разрушать ткани. Поэтому при работе с кислотами необходимо соблюдать меры предосторожности.
Если кислота попала на одежду или на поверхность тела, то её необходимо очень быстро смыть большим количеством проточной воды или нейтрализовать нашатырным спиртом.
Если кислота попала на деревянную, металлическую или на другие поверхности, то ее нейтрализуют известью, мелом или содой. Кислоты необходимо хранить в хорошо укупоренной посуде в недоступном месте для детей, и обязательно на таре должна быть бирка с названием кислоты.
Серная кислота является более сильной кислотой, чем соляная. Концентрированная серная кислота обугливает сахар, дерево, хлопок, шерсть и вызывает очень глубокие ожоги кожи.
При приготовлении раствора серной кислоты необходимо следовать следующему правилу: Кислоту льют в воду тонкой струйкой по стенке стеклянной посуды, но не наоборот.
Химические свойства кислот
1. Действие на индикаторы.
Кислоты в водных растворах изменяют окраску индикаторов.
В кислой среде фиолетовый лакмус приобретает красную окраску. Метиловый оранжевый – красную, а фенолфталеиновый – бесцветный. Если в раствор кислоты добавим по несколько капель универсального индикатора, он также поменяет окраску на красную.
Окраска индикаторов в различных средах.
2. Реакция с металлами.
Кислоты взаимодействуют с металлами, стоящими в ряду активности металлов до водорода. При этом получается соль и выделяется водород.
Металлы, расположенные в ряду активности металлов до водорода, вытесняют водород из кислот. Каждый предыдущий металл активнее, чем каждый последующий. 
Эта реакция относится к реакциям замещения.
Реакцию между простым и сложным веществами, в результате которой образуются новые простое и сложное вещества, называют реакцией замещения.
При реакциях азотной кислоты и концентрированной серной кислоты с металлами образуются соли, но водород не выделяется.
3. Реакция с основными и амфотерными оксидами с образованием соли и воды. 
Произошла реакция обмена: два сложных вещества обменялись своими составными частями.
4. Реагируют с основаниями. 

Реакция нейтрализации – реакция между кислотой и основанием, в результате которой получается соль и вода.
5.Реакция с солями.
Реакции кислот с солями не всегда возможны.
А. Кислоты реагируют с растворами солей, если в результате реакции один из продуктов выпадает в осадок. 


Б. Если кислота – продукт является летучей, происходит от газообразного соединения или разлагается с образованием газа. 


Сокращение (тв.) означает «твердое вещество», а (конц.) – «концентрированный раствор».
В. Если кислота, которая вступает в реакцию, является сильной, а кислота, которая образуется, – слабой.
Пользуясь вытеснительным рядом кислот можно предсказать течение реакции. Каждая предыдущая кислота может вытеснить из соли последующую.
Например,

но не будет происходить реакция между 


Вытеснительный ряд кислот.
Взаимодействие кислот с солями также относится к реакциям обмена.
6. Термическое разложение кислородсодержащих кислот.
Кислородсодержащие кислоты при нагревании, а угольная кислота и сернистая в обычных условиях, разлагаются с образованием соответствующих кислотных оксидов и воды:
Химические свойства кислот можно обобщить таким образом:
А. Изменяют цвет индикаторов
Б. Реагируют с металлами
В. Реагируют с основными и амфотерными оксидами
Г. Реагируют с основаниями
Д. Реагируют с солями (более слабых и летучих кислот)
Е. Некоторые кислоты разлагаются при нагревании.
В промышленности.
Наибольшее применение получили серная, соляная, азотная и ортофосфорная кислоты. Их получают на химических заводах в больших количествах.
| Кислота | Область применения |
 | Производство других кислот, солей, удобрений, красителей, лекарств, очистка нефтепродуктов. Серную кислоту, за счет ее свойств поглощать большие количества воды, используют для осушения. Применяется для приготовления аккумуляторной кислоты. |
 | Производство солей, красок, лекарств. |
 | Производство удобрений, красителей, взрывчатых веществ. |
 | Производство удобрений, моющих средств. |
Общие способы получения кислот
1. Бескислородные кислоты получают при растворении в воде газообразных соединений неметаллов с водородом. Так, например, соляная кислота получается в результате растворения газа хлороводорода 


2. Кислородсодержащие кислоты можно получить взаимодействием соответствующих кислотных оксидов с водой. 
3. Получение кислот вытеснением из солей слабых кислот сильными, летучих нелетучими, растворимых – нерастворимыми. Например, сильная соляная кислота вытесняет слабую уксусную из растворов их солей. 


Тесты подготовки к ЗНО:
Online-тест подготовки к ЗНО по химии №12 «Кислоты»