Как узнать координационное число
Основы современной координационной теории были изложены в конце прошлого века швейцарским химиком Альфредом Вернером, обобщившим в единую систему весь накопившийся к тому времени экспериментальный материал по комплексным соединениям. Им были введены понятия о центральном атоме (комплексообразователь) и его координационном числе, внутренней и внешней сфере комплексного соединения, изомерии комплексных соединений, предприняты попытки объяснения природы химической связи в комплексах.
Все основные положения координационной теории Вернера используются и в настоящее время. Исключение составляет его учение о природе химической связи, которое представляет сейчас лишь исторический интерес.
Образование комплексного иона или нейтрального комплекса можно представить себе в виде обратимой реакции общего типа:
M + n L 
В комплексных ионах комплексообразователями являются медь(II), кремний(IV), железо(II), бор(III).
Чаще всего комплексообразователем служит атом элемента в положительной степени окисления.
Отрицательные условные ионы (т.е. атомы в отрицательной степени окисления) играют роль комплексообразователей сравнительно редко. Это, например, атом азота(-III) в катионе аммония [NH 4 ] + и т.п.
Атом-комплексообразователь может обладать нулевой степенью окисления. Так, карбонильные комплексы никеля и железа, имеющие состав [Ni(CO) 4 ] и [Fe(CO) 5 ], содержат атомы никеля(0) и железа(0).
Комплексообразователь (выделен синим цветом) может участвовать в реакциях получения комплексов, как будучи одноатомным ионом, например:
так и находясь в составе молекулы:
P H 3 + H + 
B F 3 + NH 3 
В комплексной частице может быть два и более атомов-комплексообразователей. В этом случае говорят о многоядерных комплексах.
Лиганды, как правило, не связаны друг с другом, и между ними действуют силы отталкивания. В отдельных случаях наблюдается межмолекулярное взаимодействие лигандов с образованием водородных связей.
Примером гексадентатного лиганда может служить анион этилендиаминтетрауксусной кислоты:
Полидентатные лиганды могут выступать в роли мостиковых лигандов, объединяющих два и более центральных атома.
Важнейшей характеристикой комплексообразователя является количество химических связей, которые он образует с лигандами, или координационное число ( КЧ ). Эта характеристика комплексообразователя определяется главным образом строением его электронной оболочки и обусловливается валентными возможностями центрального атома или условного иона-комплексообразователя (подробнее см. >>>).
Когда комплексообразователь координирует монодентатные лиганды, то координационное число равно числу присоединяемых лигандов. А число присоединяемых к комплексообразователю полидентатных лигандов всегда меньше значения координационного числа.
Значение координационного числа комплексообразователя зависит от его природы, степени окисления, природы лигандов и условий (температуры, природы растворителя, концентрации комплексообразователя и лигандов и др.), при которых протекает реакция комплексообразования. Значение КЧ может меняться в различных комплексных соединениях от 2 до 8 и даже выше. Наиболее распространенными координационными числами являются 4 и 6.
В аквакомплексах координационное число комплексообразователя в степени окисления +II чаще всего равно 6:
Известны комплексообразователи, которые обладают практически постоянным координационным числом в комплексах разных типов. Таковы кобальт(III), хром(III) или платина(IV) с КЧ 6 и бор(III), платина(II), палладий(II), золото(III) с КЧ 4. Тем не менее большинство комплексообразователей имеет переменное координационное число. Например, для алюминия(III) возможны КЧ 4 и КЧ 6 в комплексах и
Координационные числа 3, 5, 7, 8 и 9 встречаются сравнительно редко. Есть всего несколько соединений, в которых КЧ равно 12 – например, таких как K9 [Bi(NCS) 12 ].
Лиганды, непосредственно связанные с комплексообразователем, образуют вместе с ним внутреннюю (координационную) сферу комплекса.
Так, в комплексном катионе внутренняя сфера образована атомом комплексообразователя – меди(II) и молекулами аммиака, непосредственно с ним связанными.
Обозначается внутренняя сфера квадратными скобками:
В зависимости от соотношения суммарного заряда лигандов и комплексообразователя внутренняя сфера может иметь положительный заряд, например, либо отрицательный, например, или нулевой заряд, например, как для
При растворении в воде комплексные соединения необратимо диссоциируют на ионы:
Кислоты с комплексными анионами в водном растворе подвергаются необратимому протолизу :
в котором реализуется четверная связь Re – Re: одна σ-связь, две π- связи и одна δ-связь. Особенно большое число кластерных комплексов насчитывается среди производных d-элементов.
Многоядерные комплексы смешанного типа содержат как связь комплексообразователь–комплексообразователь, так и мостиковые лиганды.
Примером комплекса смешанного типа может служить карбонильный комплекс кобальта состава [Co 2 (CO) 8 ], имеющий следующее строение:
Здесь имеется одинарная связь Co – Co и два бидентатных карбонильных лиганда CO, осуществляющих мостиковое соединение атомов-комплексообразователей.
Координационное число
Координационное число (в химии и кристаллографии) — характеристика, которая определяет число ближайших частиц (ионов или атомов) в молекуле или кристалле.
Содержание
Координационное число в химии
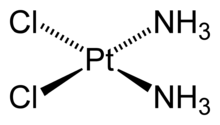
Например, в комплексной соли гексацианоферрате(III) калия K3[Fe(CN)6] координационное число иона Fe 3+ равно 6, а в цис-дихлородиамминплатине (II) (соли Пейроне) Pt(NH3)2Cl2 центральный атом платины связан с четырьмя лигандами.
Понятие координационного числа применяется также при описании структуры жидкостей и аморфных тел. В этом случае координационное число — мера ближнего порядка, среднее число ближайших соседей атома. Оно может быть дробным.
Координационное число в кристаллографии
В кристаллохимии координационное число — характеристика, которая определяет число ближайших равноудаленных одинаковых частиц (ионов или атомов) в кристаллической решётке. Прямые линии, соединяющие центры ближайших атомов или ионов в кристалле, образуют координационный многогранник, в центре которого находится данный атом.
В решётках Браве для всех узлов координационное число одинаково. Число ближайших соседей отражает плотность упаковки вещества. Чем больше координационное число, тем больше плотность и соответственно свойства вещества ближе к металлическим. Данному параметру решетки соответствует первая, вторая (соседи, следующие за ближайшими), третья и т. д. координационные группы частиц.
Для простой кубической решетки координационное число равно шести, для ОЦК — 8, ГЦК и ГП (гексагональной плотноупакованной) — 12.
См. также
Источники
Примечания
Полезное
Смотреть что такое «Координационное число» в других словарях:
КООРДИНАЦИОННОЕ ЧИСЛО — число ближайших к данному атому соседних атомов в кристаллической решётке (атомной структуре кристалла) или молекул в молекулярных кристаллах. Если центры этих ближайших соседей соединить друг с другом прямыми линиями, то получится плоская фигура … Физическая энциклопедия
КООРДИНАЦИОННОЕ ЧИСЛО — 1) в кристаллографии число ближайших к данному атому или иону соседних атомов или ионов в кристалле, находящихся от него на одинаковом расстоянии.2) В химии число лигандов, связанных с центральным ионом в комплексных соединениях … Большой Энциклопедический словарь
КООРДИНАЦИОННОЕ ЧИСЛО — одно из основных понятий кристаллохимии, означающее число атомов или ионов, окружающих любой атом или ион на ближайшем расстоянии, или в первой сфере. В гольдшмидто паулинговской кристаллохимии считалось, что К.ч. определяется соотношением… … Геологическая энциклопедия
КООРДИНАЦИОННОЕ ЧИСЛО — число ближайших к данному атому (иону) соседних атомов (ионов) в кристаллической решетке. В титаномагнетите, например, у катионов в тетраэдрических узлах подрешетки А координационное число – 4, в октаэдрических узлах подрешетки В – 6. Существуют… … Палеомагнитология, петромагнитология и геология. Словарь-справочник.
координационное число — – число лигандов, непосредственно связанных с комплексообразователем, определяемое числом свободных орбиталей в центральном атоме. Общая химия : учебник / А. В. Жолнин [1] … Химические термины
координационное число — (напр. атомов) [А.С.Гольдберг. Англо русский энергетический словарь. 2006 г.] Тематики энергетика в целом EN cooordinate numberCNcoordination number … Справочник технического переводчика
координационное число — 1) в кристаллографии число ближайших к данному атому или иону соседних атомов или ионов в кристалле, находящихся от него на одинаковом расстоянии. 2) В химии число лигандов, связанных с центральных ионом в комплексных соединениях. * * *… … Энциклопедический словарь
координационное число — [coordination number] число ближайших соседних атомов, окружающих на равных расстояниях данный атом. Металлы с ГЦК и ГПУ решеткой имеют координационное число = 12. У металлов с ОЦК решеткой координационное число = 8; Смотри также: Число число… … Энциклопедический словарь по металлургии
координационное число — (см. координация) 1) физ. число ближайших к данному атому или иону соседних атомов или ионов в кристалле (наибольшее координационное число равно 12); 2) хим. число атомов (групп атомов) или ионов, связанных хим. связью с центральным атомом в… … Словарь иностранных слов русского языка
координационное число — koordinacijos skaičius statusas T sritis Standartizacija ir metrologija apibrėžtis Atomų ar atomų grupių, tiesiogiai prisijungusių prie atomo, skaičius kompleksiniame junginyje. atitikmenys: angl. coordination number vok. Koordinationszahl, f rus … Penkiakalbis aiškinamasis metrologijos terminų žodynas
Урок №15. Комплексные соединения
Na 2 [Zn(OH) 4 ] →2Na + + [Zn(OH) 4 ] 2-
Ионы противоположного знака, связанные с комплексным ионом, образуют внешнюю сферу.
Комплексный ион состоит из комплексообразователя и лигандов и образует внутреннюю сферу (внутреннюю сферу заключают в квадратные скобки).
Координационное число зависит:
от природы центрального атома;
условий образования комплексов.
Виды комплексов
Соединения с комплексными анионами
Соединения с комплексными катионами
[Ag(NH 3 ) 2 ]Cl – хлорид диамминсеребра
[Al(H 2 O) 5 OH]SO 4 – сульфат гидроксопентаакваалюминия
[Pt(H 2 O)(NH 3 ) 2 OH] NO 3 – нитрат гидроксодиамминакваплатины (II)
Соединения без внешней сферы
[Pt(NH 3 ) 2 Cl 2 ] – дихлородиамминплатина (II)
[Co(NH 3 ) 3 Cl 3 ] – трихлоротриамминкобальт (III)
Номенклатура
в названиях комплексных ионов сначала указываются лиганды;
название комплексного иона завершается названием металла с указанием его степени окисления (римским цифрами в скобках);
в названиях комплексных катионов используются русские названия металлов;
в названиях комплексных анионов используются латинские названия металлов: Al –алюминат, Cr – хромат, Fe – феррат;
Координационный номер: что это такое, расчет, примеры
Содержание:
Это число важно, потому что оно определяет геометрию комплексов, плотность их материальных фаз и даже стереохимический (пространственный) характер их реакционной способности. Чтобы упростить его определение, любой атом, окружающий определенный центр, считается соседом.
Рассмотрим, например, пол из монет на изображении выше. Все монеты одинакового размера, и если вы посмотрите на каждую, она окружена шестью другими; то есть у них шесть соседей, и поэтому координационное число (C.N.) для монет равно 6. Эта же идея теперь распространяется на трехмерное пространство.
Если их радиусы не равны, не все они будут иметь одинаковое координационное число. Например: чем больше монета, тем больше у нее будет соседей, поскольку она сможет взаимодействовать с большим количеством монет вокруг себя. С мелкими монетами происходит обратное.
Концепция координационного числа
Ионные радиусы vs. Координационный номер
Следующее изображение иллюстрирует сказанное выше:
M 2+ в проиллюстрированном комплексе он имеет координационное число 5: он окружен 5 лигандами L. В то время как M 3+ имеет координационное число 4. Это потому, что M 3+ Поскольку они обладают большей величиной заряда, их радиус сжимается, и, следовательно, связующие L должны приближаться друг к другу, что увеличивает их электронное отталкивание.
Вот почему крупные центральные ионы, например, принадлежащие блочным металлам F, либо ко второму или третьему периоду блока d, как правило, имеют более высокие координационные числа (C.N.> 6).
Плотности
В общем, давление увеличивает координационные числа, поскольку соседи вынуждены опоясываться центральным ионом или атомом. Следовательно, материальные фазы этих веществ становятся более плотными, компактными.
Геометрии
Каждый C.N. Он связывает несколько возможных геометрий, которые размещают связующие на подходящем расстоянии таким образом, чтобы между ними было наименьшее отталкивание.
Как рассчитывается или определяется координационное число?
Поэтому координационное число предпочтительнее определять, чем рассчитывать. Как? Определение ионной или молекулярной структуры соединений. Это возможно благодаря инструментальным методам, таким как дифракция рентгеновских лучей, нейтронов или электронов.
Примеры координационных чисел
Далее и в завершение будут упомянуты некоторые примеры соединений для каждого из наиболее распространенных координационных чисел. Точно так же они расскажут, какова их геометрия.
C.N. 2
A. C.N. равен 2 означает, что центральный атом или ион имеет только двух соседей. Следовательно, мы говорим об обязательном построении линейных геометрий. Между ними у нас есть:
C.N. 3
A. C.N. равное 3 означает, что центральный атом или ион окружен тремя соседями. Затем у нас есть такие геометрии, как: тригональная плоскость (треугольник), тригональная пирамида и Т-образная форма. Примеры соединений с этим координационным числом:
— [Pt (PCy3)3], где PCy относится к лиганду трициклогексилофосфину
C.N. 4
Все эти примеры, кроме цис-PtCl2(NH3)2, имеют тетраэдрическую геометрию.
C.N. 5
A. C.N. равное 5 означает, что центральный атом или ион координирует или взаимодействует с пятью соседями. Его геометрия, как уже упоминалось, представляет собой квадратную пирамиду или тригонально-бипирамидальную форму. В качестве примеров у нас есть следующее:
C.N. 6
Это, безусловно, наиболее распространенное координационное число среди всех соединений. Помните пример с монетами с самого начала. Но вместо предпочтительной геометрии плоского шестиугольника он соответствует октаэдру (нормальному или искаженному) в дополнение к тригональной призме. Вот некоторые из многих примеров соединений с этим координационным числом:
-NaCl (да, поваренная соль)
-MoS2, обратите внимание, что C.N. для этого соединения это не 2
Другие
Есть другие координационные числа от 7 до 15. Для C.N. высокий, центральный ион или атом должен быть очень большим, иметь небольшой заряд, и в то же время лиганды должны быть очень маленькими. Некоторые примеры соединений с такими C.N. Они внизу и напоследок:
-K3[NbOF6], C.N. 7 и прикладная геометрия октаэдра
Ссылки
30 книг для быстрого и легкого изучения английского языка
Внутренняя торговля: характеристики и возрождение
Координационный номер
Содержание
Молекулы, многоатомные ионы и координационные комплексы [ править ]
Простые и банальные случаи [ править ]
Полигапто-лиганды [ править ]
Поверхности и реконструкция [ править ]
Тематические исследования [ править ]
Два наиболее распространенных аллотропа углерода имеют разные координационные числа. В алмазе каждый атом углерода находится в центре правильного тетраэдра, образованного четырьмя другими атомами углерода, координационное число равно четырем, как у метана. Графит состоит из двухмерных слоев, в которых каждый углерод ковалентно связан с тремя другими атомами углерода; атомы в других слоях находятся дальше и не являются ближайшими соседями, что дает координационное число 3. [12]
Осложнения [ править ]
В некоторых соединениях связи металл-лиганд могут не все находиться на одинаковом расстоянии. Например, в PbCl 2 координационное число Pb 2+ может составлять семь или девять, в зависимости от того, какие хлориды относятся к лигандам. У семи хлоридных лигандов расстояния Pb-Cl составляют 280–309 пм. Два хлоридных лиганда расположены дальше, с расстояниями Pb-Cl 370 пм. [13]
Некоторые металлы имеют неправильную структуру. Например, цинк имеет искаженную гексагональную плотноупакованную структуру. Регулярная гексагональная плотная упаковка сфер предсказывает, что каждый атом имеет 12 ближайших соседей и треугольный ортобикупола (также называемый антикубоктаэдром или двойниковым кубооктаэдром) координационным полиэдром. [12] [16] В цинке есть только 6 ближайших соседей в 266 пм в одной и той же плотноупакованной плоскости с шестью другими ближайшими соседями, равноудаленными, по три в каждой из плотноупакованных плоскостей выше и ниже в 291 пм. Считается разумным описать координационное число как 12, а не 6. [15] Аналогичные соображения могут быть применены к структуре регулярного куба с центрированным телом, где помимо 8 ближайших соседей есть еще 6, примерно на 15% более удаленных, [12], и в этом случае координационное число часто считается равным 14.
Использование в квазикристаллических, жидких и других неупорядоченных системах [ править ]
Координационное число систем с беспорядком не может быть точно определено.
Первое координационное число может быть определено с помощью радиальной функции распределения г ( г ): [18] [19]
Второе координационное число определяется аналогично:
Первая координационная оболочка является сферической оболочкой с радиусом между г 0 и г 1 вокруг центральной частицы исследуемого.