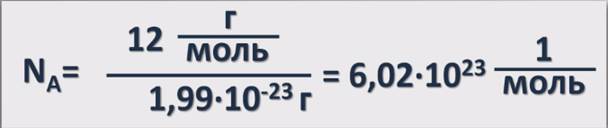Перевод из грамм в число моль и из числа моль в граммы
Калькулятор выполняет перевод из массы вещества, заданной в граммах, в количество вещества в молях и обратно.
Калькулятор ниже автоматически вычисляет молярную массу по формуле вещества и рассчитывает массу вещества в граммах или количество вещества в молях, в зависимости от выбора пользователя. Для справки также выводится молярная масса соединения и детали ее расчета
Перевод из грамм в число молей и из числа молей в граммы
И, собственно, самым сложным моментом в расчете является определение молярной массы химического соединения.
К счастью, на нашем сайте уже есть калькулятор Молярная масса соединений, который подсчитывает молярную массу химических соединений, основываясь на данных по атомной массе из справочника Таблица Менделеева. Он и используется, чтобы получить молярную массу по введенной формуле химического соединения в калькуляторе.
Внезапно русский язык
Согласно викисловарю, слово моль склоняется, т.е. моль, моля, молю, моль, молем, моле в единственном числе, и моли, молей, молям, моли, молями, молях во множественном числе.
При этом согласно Методическому указанию от 1979 года Государственного комитета СССР по стандартам, «Обозначение единиц, совпадающих с наименованиями этих единиц, по падежам и числам изменять не следует, если они помещены после числовых значений, а также в заголовках граф, боковиков таблиц и выводов, в пояснениях обозначений величин к формулам. К таким обозначениям относятся: бар, бэр, вар, моль, рад. Следует писать 1 моль, 2 моль, 5 моль и т.д. Исключение составляет обозначение «св.год», которое изменяется следующим образом: 1 св.год, 2,3,4 св.года, 5 св.лет.»
Молекулярная физика. Моль. Постоянная Авогадро. Количество вещества.
Моль — количество вещества, масса которого, выраженная в граммах, численно равна относительной атомной (молекулярной) массе.
Моль — единица количества вещества в СИ (одна из основных единиц СИ).
В 1 моле содержится столько молекул (атомов или других частиц вещества), сколько атомов содержится в 0,012 кг нуклида углерода 12 С с атомной массой 12.
Из этого определения следует, что в одном моле любого вещества содержится одно и то же число атомов или молекул.
Число это называется постоянной Авогадро и обозначается NA:
Постоянная Авогадро (число Авогадро) — это число атомов (молекул, или других структурных элементов вещества), содержащихся в 1 моле.
Постоянная Авогадро — одна из фундаментальных физических констант. Она входит в некоторые другие постоянные, например, в постоянную Больцмана.
Количество вещества.
Количество вещества — это число частиц вещества (атомов, молекул), выраженное в молях. Учитывая определение моля и числа Авогадро, можно сказать, что количество вещества v равно отношению числа молекул N в данном теле к постоянной Авогадро NA, т.е. к числу молекул в 1 моле вещества:

Как узнать количество моль
Письмо с инструкцией по восстановлению пароля
будет отправлено на вашу почту
В химической практике, имея дело с веществами, а не с отдельными атомами или молекулами, химики редко используют массы, измеряемые в атомных единицах. Масса порции реагирующих веществ или продуктов реакции чаще измеряется в граммах или в более крупных единицах.
Чтобы перейти от молекул к порциям веществ, воспользуемся единицей измерения, которая называется моль.
Химик и физик из Франции Жозеф Луи Гей-Люссак в 1808 году изучал интересную химическую реакцию, в которой в результате взаимодействия двух газов – хлороводорода и аммиака – получалось кристаллическое вещество – хлорид аммония.
Оказалось, что для реакции требуются одинаковые объемы хлороводорода и аммиака. Если одного из этих газов вначале будет больше, то по окончании реакции этот избыток оставался неиспользованным.
Гей-Люссак привел свои наблюдения в статье, но никаких выводов из них не сделал. Важные заключения через три года привел итальянский химик Амедео Авогадро. В 1811 году, в результате экспериментов и расчетов, Авогадро пришел к мысли, что равные объемы газов, находящихся при одинаковых условиях, содержат одно и то же число молекул.
Гипотеза Авогадро долго считалась спорной, поскольку не подтверждалась расчетами, основанными на ошибочном мнении о немолекулярном строении простых газообразных веществ. Однако в 1865 году австрийский физик и химик Иоганн Лошмидт предпринял попытку рассчитать число молекул газа в заданном объеме.
Когда гипотеза Авогадро была признана, ученые получили возможность правильно определять состав молекул химических соединений, рассчитывать атомные и молекулярные массы. Эти знания позволяли легко рассчитывать массовые соотношения веществ в химических реакциях. Пользоваться этими соотношения очень удобно: измеряя массу веществ в граммах, ученые как бы оперировали молекулами.
Количество вещества, численно равное относительной молекулярной массе, но выраженное в граммах, назвали грамм-молекулой или молем.
Слово «моль» придумал в начале XX века немецкий физико-химик, лауреат Нобелевской премии Вильгельм Оствальд. Слово происходит от слова «молекула».
Моль – это количество вещества, содержащее столько структурных единиц (атомов, молекул), сколько содержится атомов в 0,012 кг углерода.
Согласно Международной системе единиц СИ моль является единицей измерения особой физической величины – количества вещества. Под количеством вещества (обозначается греческой буквой ν) понимают число структурных единиц этого вещества (атомов, молекул и др.).
Самое важное заключается в том, что 1 моль любого вещества содержит одно и то же число молекул. Это число называется постоянной или числом Авогадро. Она обозначается символом NA. Постоянная Авогадро рассчитана давно и представляет собой очень большое число.
Если массу 1 моля углерода 12 г/моль разделить на массу 1 атома углерода 1,9910-23 г, то получится число, равное 6,02·1023. Поскольку это число обозначает количество частиц в 1 моле, единицы его пишут как 1/моль, моль-1 или обратный моль.
Чтобы как-то представить это число, скажем лишь, что оно больше, чем число стаканов воды, которое содержится в Мировом океане, а 6,02·1023 зёрен пшеницы имели бы массу порядка 2·1016 тонн.
Для сбора такого урожая потребовалось бы более 2 миллионов лет. Из примеров ясно: применение числа Авогадро для отсчета макротел бессмысленно. Главное его назначение – определение количества частиц (атомов и молекул) микромира и связь единиц микро и макромира.
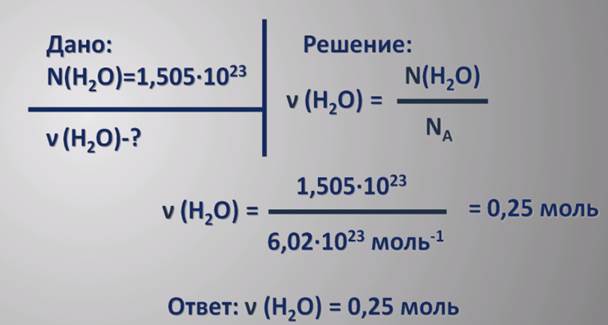
Зная количество вещества, можно судить о числе частиц в определенной его порции и брать вещества для реакций в необходимых количествах. Таким образом, химики могут определять число атомов и молекул путём взвешивания порций веществ. Приведём примеры таких расчётов. Чтобы вычислить количество вещества, зная число частиц, используем формулу 2 где ν – количество вещества в молях, N – число частиц вещества, NА – постоянная Авогадро.
Задача.Какое количество вещества содержит 1,505·1023 молекул воды?
В химии редко используется такая величина как число частиц. Гораздо легче использовать величины, которые легко измерить. Такой величиной является масса вещества. Как же связаны между собой масса и количество вещества? Зная число молекул вещества в одном моле и массу одной молекулы, можно подсчитать массу одного моля вещества. Например, известно, что масса молекулы воды равна
2,992·10-23г. Умножив ее на постоянную Авогадро, 6,02·1023 обратных молей, мы получим
18 г/моль – массу одного моля воды или молярную массу воды.
Молярной массой называется масса вещества, взятого в количестве 1 моль. Измеряется она в г/моль и обозначается латинской буквой М. Чтобы найти молярную массу вещества, нет необходимости проделывать столь сложные расчеты. Достаточно помнить, что молярная масса численно равна относительной молекулярной массе и имеет размерность г/моль.
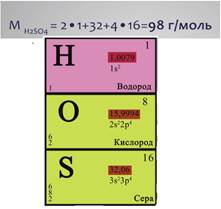
Например, относительная молекулярная масса серной кислоты Н2SО4 равна 2·1+32+4·16=98, следовательно, молярная масса серной кислоты Н2SО4 равна 98 г/моль.
Молярную массу используют для перевода количества вещества в массу и наоборот. Для расчетов используют формулу: количество вещества ν равно отношению массы вещества m к молярной массе этого вещества М.
Решим задачу. Вычислить количество вещества азотной кислоты массой 75,6 г.
Если требуется найти массу, зная количество вещества, формулу преобразуют: масса вещества m равна произведению количества вещества ν на молярную массу этого вещества М.
Моль (единица)
Моль (обозначение — моль, mol) — единица измерения количества вещества. Соответствует количеству вещества, содержащему столько специфицированных структурных единиц (атомов, молекул, ионов, электронов или любых других частиц), сколько содержится атомов в 12 граммах нуклида углерода 12 C.
Количество частиц в одном моле любого вещества постоянно и носит название числа Авогадро (NA).
Кратные и дольные единицы
Десятичные кратные и дольные единицы образуют с помощью стандартных приставок СИ.
| Кратные | Дольные | ||||||
|---|---|---|---|---|---|---|---|
| величина | название | обозначение | величина | название | обозначение | ||
| 10 1 моль | декамоль | дамоль | damol | 10 −1 моль | децимоль | дмоль | dmol |
| 10 2 моль | гектомоль | гмоль | hmol | 10 −2 моль | сантимоль | смоль | cmol |
| 10 3 моль | киломоль | кмоль | kmol | 10 −3 моль | миллимоль | ммоль | mmol |
| 10 6 моль | мегамоль | Ммоль | Mmol | 10 −6 моль | микромоль | мкмоль | µmol |
| 10 9 моль | гигамоль | Гмоль | Gmol | 10 −9 моль | наномоль | нмоль | nmol |
| 10 12 моль | терамоль | Тмоль | Tmol | 10 −12 моль | пикомоль | пмоль | pmol |
| 10 15 моль | петамоль | Пмоль | Pmol | 10 −15 моль | фемтомоль | фмоль | fmol |
| 10 18 моль | эксамоль | Эмоль | Emol | 10 −18 моль | аттомоль | амоль | amol |
| 10 21 моль | зеттамоль | Змоль | Zmol | 10 −21 моль | зептомоль | змоль | zmol |
| 10 24 моль | йоттамоль | Имоль | Ymol | 10 −24 моль | йоктомоль | имоль | ymol |
| применять не рекомендуется | |||||||
Примечание: единица измерения йоктомоль может использоваться лишь формально, так как столь малые количества вещества должны измеряться отдельными частицами (1 имоль формально равен 0,602 частицы).
| Единицы СИ |
|---|
| Основные: метр | килограмм | секунда | ампер | кельвин | кандела | моль |
| Производные: радиан | стерадиан | герц | градус Цельсия | катал | ньютон | джоуль | ватт | паскаль | кулон | вольт | ом | сименс | фарад | вебер | тесла | генри | люмен | люкс | беккерель | грэй | зиверт |
Полезное
Смотреть что такое «Моль (единица)» в других словарях:
Моль (единица кол-ва вещ-ва) — Моль, единица количества вещества, т. е. величины, оцениваемой количеством содержащихся в физической системе тождественных структурных элементов (атомов, молекул, ионов и других частиц или их специфических групп). М. равен количеству вещества… … Большая советская энциклопедия
Моль (единица кол-ва вещ-ва) — Эта статья посвящена единице измерения. См. также: насекомые моли. Моль (обозначение моль, mol) единица измерения количества вещества. Соответствует количеству вещества, содержащему столько специфицированных структурных единиц (атомов, молекул,… … Википедия
моль — 1. МОЛЬ, и; ж. Небольшая бабочка, гусеница которой является вредителем шерстяных вещей, хлебных зёрен и растений. 2. МОЛЬ, и; ж.; МОЛЬ, я; м. Спец. Лес, сплавляемый по реке брёвнами, не связанными в плот. По реке плыла м. Пробираться на лодке… … Энциклопедический словарь
Моль (значения) — Моль многозначное слово: Моль единица измерения количества вещества, Моль представитель молей (под названием «моли» объединяют в нетаксономическую группу мелких насекомых из отряда чешуекрылых). Населённые пункты Моль … … Википедия
МОЛЬ — единица количества вещества в СИ, определяемая как количество вещества, содержащее столько же формульных (структурных) единиц этого вещества (атомов, молекул, ионов, электронов и др.), сколько содержится атомов в 12 г изотопа углерода 12 (12С);… … Большая политехническая энциклопедия
МОЛЬ — • МОЛЬ (Mohl) Хуго фон (1805 1872), немецкий ботаник, пионер в исследовании анатомии и физиологии КЛЕТОК растений. Сформулировал гипотезу о том, что ядро клетки окружено гранулированным коллоидным веществом, которое в 1846 г. он назвал… … Научно-технический энциклопедический словарь
МОЛЬ — МОЛЬ, единица количества вещества в СИ. Обозначение моль. В 1 моле содержится столько молекул (атомов, ионов или каких либо других структурных элементов вещества), сколько атомов содержится в 0,012 кг 12С (углерода с атомной массой 12). число… … Современная энциклопедия
МОЛЬ — единица количества вещества СИ, обозначается моль. В 1 моле содержится столько молекул (атомов, ионов или каких либо др. структурных элементов вещества), сколько атомов содержится в 0,012 кг 12С (углерода с атомной массой 12), т. е. 6,022.1023… … Большой Энциклопедический словарь
Моль — МОЛЬ, единица количества вещества в СИ. Обозначение моль. В 1 моле содержится столько молекул (атомов, ионов или каких либо других структурных элементов вещества), сколько атомов содержится в 0,012 кг 12С (углерода с атомной массой 12). Число… … Иллюстрированный энциклопедический словарь
Моль — Эта статья посвящена единице измерения. У слова «Моль» есть и другие значения: см. Моль (значения). Моль (русское обозначение: моль; международное: mol) единица измерения количества вещества в Международной системе единиц (СИ), одна из семи … Википедия
Определение молярного объема при химических реакциях
Молярный объем — что это такое в химии
Молярный объем V m — является отношением объема вещества к его количеству, численно равен объему одного моля вещества.
Термин «молярный объем» применим по отношению к простым веществам, химическим соединениям и смесям. Величина зависит от следующих факторов:
Молярный объем вычисляют по формуле:
Молярный объем является характеристикой плотности упаковки молекул в рассматриваемом веществе. В случае простых веществ в некоторых ситуациях допустимо использовать понятие атомного объема.
Исходя из того, что объем газа определяется температурой и давлением, в процессе расчетов принято использовать объемы газов при нормальных условиях (сокращенно — н. у.). За нормальные условия принимают:
Молярный объем какого-либо газа при нормальных условиях:
Молярный объем смеси
Молярный объем смеси:
Молярный объем газов
Закон Авогадро: одинаковые количества газов при одинаковых условиях занимают одинаковый объем.
Молярный объем идеального газа вычисляют с помощью формулы, которая является выводом из уравнения состояния идеального газа.
Молярный объем идеального газа:
где T — является термодинамической температурой;
R — универсальная газовая постоянная.
Молярный объем кристаллов
Объем V я элементарной ячейки кристалла вычисляют с помощью характеристик кристаллической структуры, которые определяют на основании результатов рентгеноструктурного анализа.
Зависимость между объемом ячейки и молярным объемом:
где Z — определяет, сколько формульных единиц в элементарной ячейке.
Значения молярного объема химических элементов
Вычисление химического количества газа по его объему
Объем газа можно рассчитать по его химическому количеству. В этом случае необходимо преобразовать формулу молярного объема путем выражения из нее V :
Таким образом, объем газа равен произведению его химического количества на молярный объем. Продемонстрировать данное утверждение можно на примере. Допустим, что необходимо определить объем (н. у.) метана с химическим количеством 1,5 моль. Используя уравнение, записанное ранее, проведем вычисления:
При известном объеме газообразного вещества можно определить химическое количество рассматриваемого газа. В этом случае следует выразить из уравнения молярного объема n:
Определение объема веществ при химических реакциях
Перед тем, как приступить к расчетам объема веществ, следует ввести понятие плотности. Данный показатель определяется отношением массы вещества к его объему. Плотность измеряют в к г / м 3 (или г/л, г/мл). В случае газообразных веществ плотность принимает очень маленькие значения. Упростить расчеты химических реакций можно, если рассматривать отношение плотностей газов.
Относительной плотностью газа В по газу А называют величину, равную отношению плотностей рассматриваемых веществ или отношению молярных масс этих газов.
Данный параметр обозначают D A ( B ) и определяют по формуле:
В связи с тем, что в расчете относительной плотности используют величины одинаковой размерности, данный параметр является безразмерной величиной. Определить относительную плотность газообразных веществ по некому газу можно с помощью отношения молярных масс этих газов. Например, относительная плотность кислорода по водороду составляет:
Согласно закону Авогадро, в равных объемах различных газов, которые существуют при одинаковых температурах и давлениях, содержится одно и то же количество молекул. Данная гипотеза была представлена в 1811 году в Турине профессором физики Амедео Авогадро.
Подтверждение теория нашла во множестве экспериментальных опытах. Закон получил название закона Авогадро и стал в дальнейшем количественной основой современной химии. Закон Авогадро в точности реализуем в случае идеального газа. С увеличением разреженности газообразного вещества повышается точность расчетов по этому закону применительно к данному реальному газу.
Первое следствие из закона Авогадро: один моль (одинаковое количество молей) любого газа при одинаковых условиях занимает одинаковый объем.
Исходя из закона Авогадро, одинаковое число молекул какого-либо газа занимает при одинаковых условиях один и тот же объем. Наряду с тем, 1 моль какого-то вещества включает в себя (согласно определению) одинаковое количество частиц (к примеру, молекул). Таким образом, при определенных температуре и давлении 1 моль любого вещества в газообразном состоянии занимает один и тот же объем.
Если условия соответствуют нормальным, то есть температура равна 0 °C (273,15 К), и давление составляет 101,325 кПа, объем 1 моль газа соответствует 22,413 962(13) л. Данная физическая константа является молярным объемом идеального газа и обозначается Vm.
Вычислить молярный объем при температуре и давлении, отличных от нормальных условий, можно с помощью уравнения Клапейрона:
Второе следствие из закона Авогадро: молярная масса первого газа равна произведению молярной массы второго газа на относительную плотность первого газа ко второму.
Как найти объемные отношения газов в смеси
В процессе вычисления объемных отношений газов, участвующих в химических реакциях, используют закон Гей-Люссака (химический закон объемных отношений). В англоязычной литературе данный закон можно встретить под названием закона Шарля.
Закон Гей-Люссака — закон, демонстрирующий пропорциональную зависимость между объемом газообразного вещества и абсолютной температурой при постоянном давлении (то есть в изобарном процессе).
Закон получил название в честь французского физика и химика Жозефа Луи Гей-Люссака.
Математическое выражение закона Гей-Люссака:
В том случае, когда известно состояние газа при постоянном давлении и двух разных температурах, закон допустимо записывать таким образом:
По итогам химических реакций атомы не исчезают и не возникают. В результате таких процессов происходит их перегруппировка. Количество атомов до реакции и после ее протекания не меняется, что отличает их от молекул. Данное условие учитывают, расставляя стехиометрические коэффициенты в уравнениях химических реакций.
Коэффициенты в уравнениях реакций демонстрируют числа объемов газов, которые реагируют и образовываются. К примеру, 2 объема водорода и 1 объем кислорода дают 2 объема пара воды:
2 H 2 + O 2 = 2 H 2 O
V ( Н 2 ) : V ( N 2 ) : V ( N H 3 ) = 3 : 2 : 1
С другой стороны, данные соотношения справедливы лишь в случае веществ, которые участвуют в одной и той же химической реакции. Когда реагент принимает участие в двух параллельных реакциях, его химические количества в данных процессах не связаны и могут принимать любые значения.
n — количество газа.
Выразить молярный объем газов можно в л/моль:
В данной таблице использованы следующие обозначения: