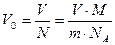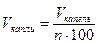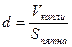Методы определения размеров молекул



В молекулярной физике главные «действующие лица» — это молекулы, невообразимо маленькие частицы, из которых состоят все на свете вещества. Ясно, что для изучения многих явлений важно знать, каковы они, молекулы. В частности, каковы их размеры.
Когда говорят о молекулах, их обычно считают маленькими упругими твердыми шариками. Следовательно, знать размер молекул, значит знать их радиус или диаметр.
Несмотря на малость молекулярных размеров, физики сумели разработать множество способов их определения. В одном используется свойство некоторых (очень немногих) жидкостей растекаться в виде пленки толщиной в одну молекулу. Вдругом, размер частицы определяется с помощью сложного прибора – ионного проектора.
Строение молекул изучают различными экспериментальными методами. Электронография, нейтронография и рентгеновский структурный анализ позволяют получать непосредственную информацию о структуре молекул. Электронографии, метод, исследующий рассеяние электронов на пучке молекул в газовой фазе, позволяет рассчитать параметры геометрической конфигурации для изолированных сравнительно простых молекул. Нейтронография и рентгеновский структурный анализ ограничены анализом структуры молекул либо отдельных упорядоченных фрагментов в конденсированной фазе. Рентгенографические исследования кроме указанных сведений дают возможность получить количественные данные о пространственном распределении электронной плотности в молекулах.
Спектроскопические методы основаны на индивидуальности спектров химических соединений, которая обусловлена характерным для каждой молекулы набором состояний и отвечающих им энергетических уровней. Эти методы позволяют проводить качественный и количественный спектральный анализ веществ.
Разнообразную информацию о строении и свойствах молекул дает изучение их поведения во внешних электрических и магнитных полях.
Существуют, однако, очень простые способы определения размеров молекул:
1 способ. Основан на том, что молекулы вещества, когда оно находится в твердом или жидком состоянии, можно считать плотно прилегающими друг к другу. В таком случае для грубой оценки можно считать, что объем V некоторой массы m вещества просто равен сумме объемов содержащихся в нем молекул. Тогда объем одной молекулы мы получим, разделив объем V на число молекул N.
Число молекул в теле массой m равно, как известно, 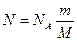
В это выражение входит отношение объема вещества к его массе. Обратное же отношение 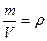
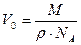
Плотность практически любого вещества можно найти в доступных всем таблицах. Молярную массу легко определить, если известна химическая формула вещества.
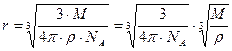
Описанный способ определения радиусов молекул не может быть точным уже потому, что шарики нельзя уложить так, чтобы между ними не было промежутков, даже если они соприкасаются друг с другом. Кроме того, при такой «упаковке» молекул – шариков были бы невозможны молекулярные движения. Тем не менее, вычисления размеров молекул по формуле, приведенной выше, дают результаты, почти совпадающие с результатами других методов, несравненно более точных.
2 способ. Метод Ленгмюра и Дево. В данном методе исследуемая жидкость должна растворяться в спирте (эфире) и быть легче воды, не растворяясь в ней. При попадании капли раствора на поверхность воды спирт растворяется в воде, а исследуемая жидкость образует пятно площадью S и толщиной d (порядка диаметра молекул).
Если допустить, что молекула имеет форму шара, то объем одной молекулы равен:
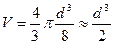
Необходимо определить диаметр молекулы d. В микропипетку набрать 0,5 мл раствора и, расположив ее над сосудом, отсчитать число капель n, содержащихся в этом объеме. Проделав опыт несколько раз, найти среднее значение числа капель в объеме 0,5 мл, а затем подсчитать объём исследуемой жидкости в капле: 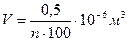

В ванну налить воду толщиной 1 – 2 см. Насыпать тальк тонким слоем на лист бумаги, ударяя слегка пальцем по коробочке. Расположив лист бумаги выше и сбоку от ванны на расстоянии 10 – 20 см, тальк сдуть с бумаги. На поверхность воды в ванне из пипетки капнуть одну каплю раствора. Линейкой измерить, средний диаметр образовавшегося пятна D и подсчитываю его площадь. Опыт повторить 2- 3 раза, а затем подсчитать диаметр молекул d.
Ход эксперимента:
1. Определение объёма капли растительного масла.
В мерный цилиндр (мензурку) накапать 190 капель масла и определить объём их. Используя формулу для определения объёма1 капли масла из метода Ленгмюра и Дево (2 способ), рассчитать объем капли.
2. Определение площади масляного пятна.
Для того, чтобы получить масляное пятно провести несколько экспериментов.
В ванну размером 40×30 см необходимо налить воду и капнуть 1 каплю растительного масла, а затем наблюдать, как расплывается пятно, когда оно перестанет расплываться – измерить его диаметр.
| № | Условия проведения эксперимента | Что увидели | Диаметр пятна (D, см) |
| 1 | В ванну налили холодную воду | ||
| 2 | Воду нагрели до 40 0 С и на поверхность насыпали тальк (измельчённый мел) | ||
| 3 | Воду нагрели до 40 0 С и добавили перманганат калия. |
Для определения площади пятна использовать формулу: 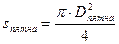
3. Определение диаметра молекулы растительного масла.
Используем формулу:
Учебники
Журнал «Квант»
Общие
Кикоин А.К. Простой способ определения размеров молекул // Квант. — 1983. — № 9. — C.29-30.
По специальной договоренности с редколлегией и редакцией журнала «Квант»
В молекулярной физике главные «действующие лица» — это молекулы, невообразимо маленькие частицы, из которых состоят все на свете вещества. Ясно, что для изучения многих явлений важно знать, каковы они, молекулы. В частности каковы их размеры.
Когда говорят о молекулах, их обычно считают маленькими упругими твердыми шариками. Следовательно, знать размер молекул значит знать их радиус.
Несмотря на малость молекулярных размеров, физики сумели разработать множество способов их определения. В «Физике 9» рассказывается о двух из них. В одном используется свойство некоторых (очень немногих) жидкостей растекаться в виде пленки толщиной в одну молекулу. В другом размер частицы определяется с помощью сложного прибора — ионного проектора.
Существует, однако, очень простой, хотя и не самый точный, способ вычисления радиусов молекул (или атомов) Он основан на том, что молекулы вещества, когда оно находится в твердом или жидком состоянии, можно считать плотно прилегающими друг к другу. В таком случае для грубой оценки можно считать, что объем V некоторой массы m вещества просто равен сумме объемов содержащихся в нем молекул. Тогда объем одной молекулы мы получим, разделив объем V на число молекул N.
Число молекул в теле массой m равно, как известно, \(
N_a \frac
В это выражение входит отношение объема вещества к его массе. Обратное же отношение \(
\frac
Плотность практически любого вещества можно найти в доступных всем таблицах. Молярную массу легко определить, если известна химическая формула вещества.
Объем одной молекулы, если считать ее шариком, равен \(
откуда мы и получаем выражение для радиуса молекулы:
Описанный способ определения радиусов молекул не может быть точным уже потому, что шарики нельзя уложить так, чтобы между ними не было промежутков, даже если они соприкасаются друг с другом. Кроме того, при такой «упаковке» молекул- шариков были бы невозможны молекулярные движения. Тем не менее вычисления размеров молекул по формуле, приведенной выше, дают результаты, почти совпадающие с результатами других методов, несравненно более точных.
Определение средней длины свободного пробега и эффективного диаметра молекулы воздуха
Лабораторная работа 2.8
ОПРЕДЕЛЕНИЕ СРЕДНЕЙ ДЛИНЫ СВОБОДНОГО ПРОБЕГА И ЭФФЕКТИВНОГО ДИАМЕТРА МОЛЕКУЛЫ ВОЗДУХА.
Согласно молекулярно-кинетической теории хаотическое молекулярное движение является физической причиной наблюдаемых в газах явлений переноса. Хотя величины скоростей молекул относительно велики и могут достигать сотен метров в секунду, процессы переноса совершаются сравнительно медленно, потому что в явлениях переноса важную роль играют не только скорости молекул, но и столкновения между ними, которые препятствуют свободному движению молекул, заставляют их двигаться не прямолинейно, а зигзагообразно.
Силы взаимодействия молекул становятся заметными лишь при малых расстояниях между ними. Поэтому можно считать, что в газах на пути свободного пробега молекулы движутся прямолинейно и равномерно. Отклонение молекул от прямолинейных траекторий их движения происходит только при достаточном сближении. То минимальное расстояние между центрами двух молекул, на котором под действием сил отталкивания происходит явление, подобное удару, называется эффективным диаметром молекулы.
Расстояние, которое проходит молекула между двумя последовательными столкновениями, называют длиной свободного пробега молекулы. В связи с тем, что молекул много, а длины свободного пробега их несколько отличаются друг от друга, в расчетах используют среднюю длину свободного пробега молекул.
Основные количественные данные для определения длины свободного пробега газовых молекул и их эффективных диаметров были получены из исследований явлений переноса – диффузии, теплопроводности и вязкости. Скорость выравнивания концентраций, температур или количества движения газа зависит от характера столкновений молекул при их тепловом движении. Поэтому изучение явлений переноса дает возможность определить основные величины, характеризующие столкновения – длину свободного пробега и эффективный диаметр молекулы.
Молекулярно-кинетическая теория позволила получить формулы, в которых макроскопические параметры газа (давление, температура) связаны с его микропараметрами (размер молекулы, масса молекулы, ее средняя тепловая скорость). Пользуясь этими формулами, можно при помощи легко измеряемых параметров: давления, температуры, коэффициента внутреннего трения – получить интересующие нас микропараметры: диаметр молекулы, ее скорость и т. д.

Сосуд на три четверти заполняют водой. Если открыть кран, то вода сначала будет выливаться непрерывной струей, а потом цепью из отдельных капель. Давление воздуха в сосуде 4 уменьшится и в капилляре 6 установится стационарное течение воздуха.
Из молекулярно-кинетической теории известно, что вязкость идеального газа равна
Однако для реальных газов учет сил межмолекулярного взаимодействия приводит к формуле:

где 


Из формулы (1) следует, что

Вязкость можно определить, воспользовавшись известной формулой Пуазейля, выражающей вязкость через объем газа, протекающего через сечение трубки за определенное время и требуемую для этого разность давлений на концах трубки (капилляра):

где V — объем протекающего газа, r — радиус трубки (капилляра), l — длина трубки (капилляра), Δ p — разность давлений на концах трубки, обуславливающая течение газа в ней,
τ — время, в течение которого вытекает данный объем газа.
Все величины, входящие в эту формулу, легко поддаются измерению.
Средняя арифметическая скорость молекул идеального газа по молекулярно-кинетической теории равна:

где R — универсальная газовая постоянная, Т — абсолютная температура, μ — молярная масса газа.
Плотность r газа находим из уравнения Менделеева-Клапейрона

где р — давление газа.
Подставив выражения (3, 4, 5) в уравнение (2) получим:

Эффективный диаметр молекулы можно вычислить из формулы для средней длины свободного пробега

где n — число молекул в единице объема при данных условиях,
d — эффективный диаметр молекулы.
Число молекул в единице объема при данных условиях можно выразить из основного уравнения кинетической теории газа:

где k – постоянная Больцмана.
Используя формулы (7) и (8), получаем выражение для эффективного диаметра молекулы газа

По формулам (6) и (9) рассчитывают соответственно длину свободного пробега молекулы и ее эффективный диаметр.
Принадлежности и приборы: сосуд с дистиллированной водой, секундомер, стакан, аналитические весы, разновесы, барометр, термометр.
1. Взвесить на весах пустой стакан ( m 1 ).
2. Открыть кран и, когда вода начнет вытекать из сосуда каплями, подставить предварительно взвешенный стакан и одновременно включить секундомер.
3. Тут же заметить по шкале высоту ( h 1 ) уровня воды в сосуде.
5. Заметить новый уровень воды ( h 2 ).
6. Взвесить стакан с водой ( m 2 ) и по массе вытекшей воды определить ее объем 
7.
 |
Разность давлений, заставляющая воздух втекать в сосуд, может быть найдена по формуле:
8. Измерить температуру ( t 1 ) по комнатному термометру.
9. Определяется по барометру атмосферное давление (р1).
10. Результаты измерений занести в таблицу 1.
11. Опыт повторить три раза.
12. По формуле (6) рассчитать среднюю длину свободного пробега.
13. По среднему значению длины свободного пробега найти эффективный диаметр молекул воздуха по формуле (9).
14. Записать окончательные результаты в виде:

Таблица 1.
Измеряем длину молекулы
Понятно, что мы не сможем непосредственно измери ть такую малую частичку вещества. Мы проведем опыт, из которого путем простых расчетов можно определить размер молекул. Вы, конечно, видели на поверхности воды тонкие цветные пленки, образуемые нефтепродуктами (смазочные масла, дизельное топливо и т.
Но есть ли у нас гарантия, что молекулы машинного масла растеклись по воде в один слой? Ведь только в этом случае толщина пленки будет соответствовать размеру молекул. Такой гарантии у нас нет, и вот почему. Молекулы, входящие в состав машинного масла, называют гидрофобными (в переводе с греческого «гидрофобные» — «боящиеся воды»). Они довольно хорошо «сцепляются» между собой, очень неохотно — с молекулами воды. Если вещество, подобное машинному маслу, налить на поверхность воды, оно образует на ней довольно толстую (по молекулярным меркам) пленку, состоящую из сотен и даже тысяч молекулярных слоев. Помимо того, что подобные расчеты любопытны и сами по себе, они имеют большое практическое значение. Например, по сей день не удается избежать аварий огромных танкеров, перевозящих нефть за тысячи километров от места ее добычи. В результате такой аварии в море может вылиться огромное количество нефти, что губительно скажется на живых организмах. Нефть более вязкая по сравнению с машинным маслом, поэтому ее пленка на водной поверхности может оказаться несколько толще. Так, в одной из аварий вылилось 120 000 тонн нефти, которая покрыла площадь 500 км3. Как показывает несложный расчет, средняя толщина такой пленки равна 200 мкм. Толщина пленки зависит как от сорта нефти, так и от температуры воды: в холодных морях, где нефть делается более густой, пленка толще, в теплых морях, где нефть становится менее вязкой, — тоньше. Но в любом случае авария большого танкера, когда в море попадают десятки тысяч тонн нефти, — это катастрофа. Ведь если вся пролитая нефть растечется тонким слоем, то образуется пятно огромной площади, и ликвидировать такую пленку чрезвычайно трудно.
А можно ли заставить вещество растекаться по воде так, чтобы образовался всего один слой молекул (такая пленка называется мономолекулярной)? Оказывается, это возможно, только вместо машинного масла или нефти надо взять другое вещество.
Вещества, которые ведут себя таким образом, называют поверхностно-активными. К ним относятся, например, мыло и другие моющие средства; олеиновая кислота, входящая в состав подсолнечного масла; паль-митиновый спирт, который входит в состав пальмового масла и китового жира. Растекание таких веществ по поверхности воды дает значительно более тонкие пленки, чем машинное масло. Это явление было известно давно, подобные опыты проводили еще в XVIII веке. Нотолько в конце XIX — начале XX столетия в результате экспериментов, проведенных английским физиком Джоном Уильямом Рэлеем (1842—1919), немецким физиком Вильгельмом Конрадом Рент- геном (1845—1923) и рядом других ученых, было показано, что толщина пленки может достигать таких малых размеров, которые сопоставимы с размерами отдельных молекул.
В одном из таких опытов английский химик НеЙл Кенсингтон Адам
Как узнать диаметр молекулы
Размер молекулы
Шестьдесят лет назад лорд Рэлей наблюдал за растеканием масла по воде. В то время, когда ученые строили различные предположения о размерах молекул, он догадался, что самый тонкий слой масла, который может полностью покрыть водную поверхность, будет иметь толщину как раз в одну молекулу, и решил определить эту толщину. Рэлей представил себе растекание капли масла как хаотическое движение молекул, карабкающихся друг на друга и сваливающихся назад, пока каждая не достигнет поверхности воды и не сможет прицепиться к воде (эти масла состоят из молекул с длинной цепью, на одном конце которых находится химическая группа, имеющая сродство к воде). Как только все молекулы масла расположатся таким способом, они будут держаться в виде мономолекулярного покрова и перестанут стремиться к дальнейшему растеканию (фиг. 130).
Фиг. 130. Масло на воде.
Капля масла, нанесенная на чистую поверхность воды, растекается и покрывает ее слоем толщиной в одну молекулу. Молекулы масла, вероятно, стоят «дыбом» подобно ворсу на ковре.
Если масла как раз достаточно для данной поверхности воды, слой будет иметь толщину в одну молекулу, и все молекулы будут плотно упакованы по вертикали, подобно ворсинкам бархата. При меньшем количестве масла останутся участки открытой воды. Если масла будет
Лорд Рэлей вымыл и заполнил водой круглый большой таз, имевший 82 см в поперечнике. На поверхность воды он поместил взвешенную каплю масла и наблюдал, как оно растекается и закрывает всю поверхность. Затем он опять взял чистую воду и каплю меньшего размера, затем еще меньшую, пока не дошел до такой капли, которая уже не могла полностью закрыть всю поверхность. Как же он обнаружил, что закрыта не вся поверхность?
Если перед опытом распылить на поверхности порошок, можно изменить свойства поверхности. Поэтому Рэлей после масла распылял камфару (помните детскую забаву?). Пока поверхность воды была полностью покрыта маслом, камфара не находила чистой воды, по которой она могла бы танцевать, но когда капля масла была мала, на поверхности открывались участки чистой воды.
Условия приведенной ниже задачи 5 следуют за ходом вычислений Рэлея. Используя результаты его измерений, определите размеры молекул масла.
Задача 5. Измерение размеров молекулы
Рэлей наносил каплю оливкового масла на чистую воду в большом сосуде. Для простоты примем, что сосуд был прямоугольным с размером зеркала воды 0,55 м х 1,00 м (это даст ту же площадь, что и в круглом тазу, взятом Рэлеем).
Движение камфары показало, что масла как раз достаточно для покрытия всей поверхности (капля масла весит 8 /10 мг, или 0,00000080 кг). Плотность масла равна 900 кг/м 3 (что составляет 0,90 от плотности воды). Предположим, что плотность остается такой же и в очень тонкой пленке.
(Помните, что поскольку масло менее плотно, чем вода, его объем должен быть больше объема той же массы воды.)
а) Определите толщину масляной пленки, образующейся при растекании капли по воде.
б) Допустим, что Релей был прав и пленка, достаточная для остановки движений камфары, имеет толщину в одну молекулу. Поверим химикам, что это масло имеет «длинные» молекулы, один конец которых сильно притягивается водой. Какой вывод можно сделать из вопроса (а) относительно размеров молекул?
Длина молекул очень мала; чтобы образовать линию в 1 см их требуются миллионы. В те времена, когда Рэлей производил свои измерения, ученые делали грубые, поспешные предположения о размере и массе молекул; их косвенные догадки основывались на трении в газах, на рассеянии солнечного света в небе молекулами и на некоторых сомнительных электрических аргументах. Здесь же был поразительно простой эксперимент и, вероятно, надежный.
С тех пор метод был улучшен и обобщен многими, особенно Ленгмюром в США. Оливковое масло, которое применял Рэлей, было неопределенной смесью маслянистых веществ. Позднейшие исследователи применяли чистые химические соединения, часто используя несколько членов «гомологического ряда» (или, иначе, химической семьи). Например, Ленгмюр применял «жирные кислоты». Их получают из природных жиров и масел, и они дают мыло, соединяясь с натрием или калием. Они имеют длинные молекулы с одним инертным, а другим «кислым» концом, который притягивается водой. Существует целый ряд таких соединений, причем молекула каждого представителя этого ряда больше своего предшественника на один атом углерода и два атома водорода. Очень давно химики изобразили молекулы различных членов этих рядов структурными формулами, подобными трем приведенным на стр. 222.
Грубой аналогией такого представления является стадо свиней у длинной кормушки. Подобно тому как один конец молекулы растительного масла «любит» воду, голова свиньи ткнется к пище, свиньи карабкаются и толкаются, пока все не достигнут кормушки. Если стадо слишком велико, неудовлетворенные будут ожидать в стороне (подобно толстым каплям избыточного масла на воде). Если число свиней будет подобрано точно по длине кормушки, они образуют слой в одно животное, причем все расположатся перпендикулярно кормушке. Если свиней слишком мало, то они расположатся произвольно и у кормушки останутся свободные места.